Van-der-Waals-Kräfte
-
01.5 Homologe Reihe der Alkane
Was du auf dieser Seite lernst
Die homologe Reihe der Alkane ordnet alle gesättigten Kohlenwasserstoffe nach ihrer Kettenlänge. Du lernst die allgemeine Formel CₙH₂ₙ₊₂, siehst wie sich Strukturformel, Halbstrukturformel und Aggregatzustand systematisch ändern – und verstehst, warum der Siedepunkt mit steigender Kettenlänge zunimmt.
Grundlagen aus 1.1 und 1.4
Strukturformeln, Halbstrukturformeln und Konstitutionsisomerie hast du bereits an Methan und Butan kennengelernt: → 1.1 Methan · → 1.4 Butan & Isomerie
(homo = gleich, logos = Stoff)
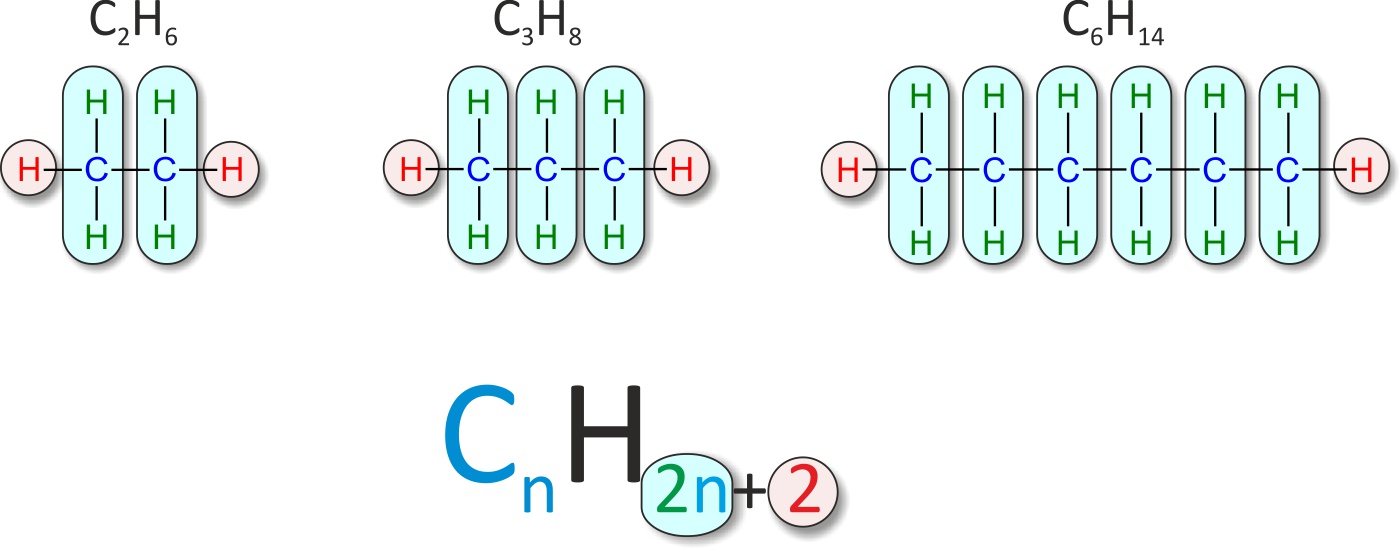
Allgemeine Summenformel der homologen Reihe:
↑ Zum Vergrößern klicken
✕
Definition – Homologe Reihe
Eine Reihe organischer Verbindungen, deren aufeinanderfolgende Glieder sich jeweils um eine bestimmte Atomgruppe – z. B. eine –CH₂– Gruppe – unterscheiden, nennt man homologe Reihe. Für Alkane gilt die allgemeine Summenformel CnH2n+2.
Wichtigste Eigenschaften aller Alkane:
- Brennbar (bei vollständiger Verbrennung entstehen CO2 und H2O)
- Dichte < 1 g/cm³ (leichter als Wasser)
- In Wasser unlöslich (nur Spuren); untereinander in jedem Verhältnis mischbar
Die homologe Reihe der Alkane (Übersicht)
Name Summenformel Strukturformel Halbstrukturformel Aggregatzustand Methan CH4 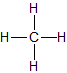
CH4 gasförmig Ethan C2H6 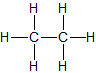
CH3–CH3 gasförmig Propan C3H8 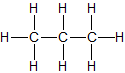
CH3–CH2–CH3 gasförmig n-Butan C4H10 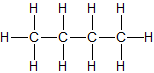
CH3–CH2–CH2–CH3 gasförmig n-Pentan C5H12 
CH3–(CH2)3–CH3 flüssig n-Hexan C6H14 
CH3–(CH2)4–CH3 flüssig n-Heptan C7H16 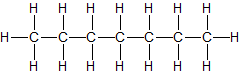
CH3–(CH2)5–CH3 flüssig n-Octan C8H18 
CH3–(CH2)6–CH3 flüssig n-Nonan C9H20 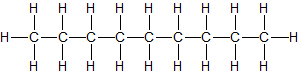
CH3–(CH2)7–CH3 flüssig n-Decan C10H22 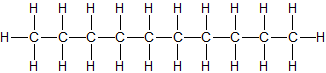
CH3–(CH2)8–CH3 flüssig n-Undecan C11H24 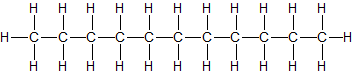
CH3–(CH2)9–CH3 flüssig n-Dodecan C12H26 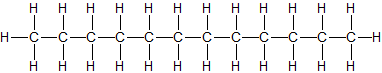
CH3–(CH2)10–CH3 flüssig … (C₁₃ bis C₁₆ flüssig) n-Heptadecan C17H36 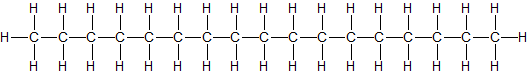
CH3–(CH2)15–CH3 fest
Auf einen Blick – Homologe Reihe der Alkane
Allgemeine Formel
CₙH₂ₙ₊₂ – jedes folgende Glied enthält eine –CH₂–-Gruppe mehr als das vorherige. Das verbindet alle Alkane zur homologen Reihe.
Aggregatzustände
C₁–C₄: gasförmig · C₅–C₁₆: flüssig · ab C₁₇: fest. Der Siedepunkt steigt mit wachsender Kettenlänge gleichmäßig an.
ZMK und Siedepunkt
Zwischen Alkanen wirken nur Van-der-Waals-Kräfte. Längere Kette = größere Moleküloberfläche = stärkere VdW-Kräfte = höherer Siedepunkt.
Eigenschaften
Alle Alkane sind brennbar, unpolar, in Wasser unlöslich und besitzen eine Dichte < 1 g/cm³. Chemisch reagieren sie wegen starker Einfachbindungen kaum.
Häufige Fragen – Homologe Reihe der Alkane
Was ist eine homologe Reihe und was verbindet die Glieder?
Eine homologe Reihe ist eine Gruppe organischer Verbindungen, deren aufeinanderfolgende Glieder sich jeweils um eine –CH₂–-Gruppe unterscheiden. Alle Glieder haben die gleiche allgemeine Summenformel (CₙH₂ₙ₊₂ für Alkane), ähnliche chemische Eigenschaften und kontinuierlich variierende physikalische Eigenschaften (Siedepunkt, Dichte etc.).
Warum wechselt der Aggregatzustand von gasförmig über flüssig zu fest?
Mit steigender Kettenlänge wächst die Moleküloberfläche. Über diese Fläche wirken Van-der-Waals-Kräfte – je größer die Fläche, desto stärker die Anziehung zwischen den Molekülen. Ab einer bestimmten Kettenlänge reicht die Wärmeenergie bei Raumtemperatur nicht mehr aus, die Moleküle voneinander zu trennen: C₁–C₄ gasförmig · C₅–C₁₆ flüssig · ab C₁₇ fest. → Eigenschaften der Alkane
Wie leitet man die Halbstrukturformel eines Alkans aus der Summenformel ab?
Man schreibt das Kohlenstoffgerüst in einer Kette und ergänzt H-Atome so, dass jedes C-Atom vierwertig ist: Die beiden Endgruppen sind immer CH₃–, jede mittlere Gruppe ist –CH₂–. Beispiel n-Hexan (C₆H₁₄): CH₃–(CH₂)₄–CH₃. Die Klammernotation (CH₂)ₙ spart Schreibarbeit bei langen Ketten.
Warum sind Alkane in Wasser unlöslich?
Alkane sind unpolare Moleküle – es gibt keine Partialladungen und keine Wasserstoffbrückenbindungen. Wasser dagegen ist polar und bildet starke Wasserstoffbrücken zwischen seinen Molekülen. Ein unpolares Alkan könnte diese Netzstruktur nicht ersetzen, daher ist das Einbringen energetisch ungünstig – „similia similibus solvuntur" (Gleiches löst Gleiches). In anderen unpolaren Lösungsmitteln (Benzin, Ether) lösen sich Alkane dagegen gut.
Wie berechnet man die Summenformel eines Alkans für beliebiges n?
Mit der allgemeinen Formel CₙH₂ₙ₊₂: Einfach n einsetzen.
Beispiel n = 8 (Octan): C₈H₂·₈₊₂ = C₈H₁₈ ✓
Umgekehrt: Aus der Summenformel C₁₂H₂₆ folgt 2n+2 = 26 → n = 12 → Dodecan.
Kontrolle: Molare Masse = 12·12 + 26·1 = 170 g/mol.Lernkarten – Homologe Reihe der Alkane
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die allgemeine Summenformel der Alkane? Worum unterscheiden sich je zwei aufeinanderfolgende Glieder?
Allg. Formel: CₙH₂ₙ₊₂
Aufeinanderfolgende Glieder unterscheiden sich um eine –CH₂–-Gruppe.
→ Deshalb heißen sie homologe Reihe.2Ab welcher Kettenlänge sind Alkane bei Raumtemperatur flüssig? Ab wann fest?
C₁–C₄: gasförmig
C₅–C₁₆: flüssig
ab C₁₇: fest
Ursache: stärkere Van-der-Waals-Kräfte mit wachsender Kettenlänge3Gib Name, Summenformel und Halbstrukturformel für das Alkan mit n = 5 an.
n = 5 → n-Pentan
Summenformel: C₅H₁₂
(2·5+2 = 12 H ✓)
Halbstrukturformel:
CH₃–CH₂–CH₂–CH₂–CH₃
oder CH₃–(CH₂)₃–CH₃4Warum steigt der Siedepunkt in der homologen Reihe der Alkane mit zunehmender Kettenlänge?
Längere Kette → größere Moleküloberfläche
→ stärkere Van-der-Waals-Kräfte
→ mehr Energie nötig zur Trennung der Moleküle
→ höherer Siedepunkt5Ein Alkan hat die Summenformel C₁₀H₂₂. Wie heißt es? Wie lautet die Halbstrukturformel? Welchen Aggregatzustand hat es bei Raumtemperatur?
C₁₀H₂₂ → n = 10 → n-Decan
Halbstrukturformel:
CH₃–(CH₂)₈–CH₃
Aggregatzustand: flüssig
(C₅–C₁₆ sind bei RT flüssig)Weiter im Kapitel Alkane
← 1.4 Butan → 1.6 Genfer Nomenklatur → 1.7 Eigenschaften
🔁 Grundlagen: 1.1 Methan · 1.4 Butan & Isomerie
📚 Vertiefung: 2.1 Ethen – Homologe Reihe der Alkene · Siedepunkte und ZMK (Carbonsäuren) -
01.7 Struktur und Eigenschaften der Alkane
Was du auf dieser Seite lernst
Die Struktur der Alkane bestimmt ihre Eigenschaften. Du lernst, warum Alkane reaktionsträge sind, welche zwischenmolekularen Kräfte (ZMK) zwischen ihren Molekülen wirken und was das für Siedepunkt, Schmelzpunkt und Löslichkeit bedeutet.
Grundlagen aus der 9. Klasse
Polare und unpolare Bindungen sowie zwischenmolekulare Kräfte (ZMK) hast du bereits in der 9. Klasse kennengelernt:
→ Polare und unpolare Atombindung (Kl. 9) · → Elektrische Dipole (Kl. 9)1.7 Struktur und Eigenschaften der Alkane
1.7.1 Bindungsverhältnisse
a) Bindungsverhältnisse im Molekül lassen bestimmte chemische Verhaltensweisen voraussagen:
- sehr starke Einfachbindung
→ reaktionsträge - fast unpolare Atombindung
→ normalerweise keine Reaktion als Säure (auch keine Eigenprotolyse), da kein Proton abgespalten wird.
→ bei starkem Erhitzen bzw. starkem Angriff kommt es zur symmetrischen (radikalischen, homolytischen) Spaltung der Bindung.
- keine freien Elektronenpaare
→ kann nicht als Base reagieren (kann kein Proton aufnehmen) - keine Elektronenpaarlücke
→ kann nicht als elektrophiles Teilchen reagieren b) Bindungen bzw. Kräfte zwischen den Molekülen (ZMKs) sind verantwortlich für die physikalischen Eigenschaften (Siedetemperatur, Schmelztemperatur, Löslichkeit etc.):
- nur van-der-Waals-Kräfte
- keine Wasserstoffbrücken
- keine Dipol-Dipol-Wechselwirkungen
- Siedepunkt ist niedrig (steigt mit der Molekülgröße)
- Schmelzpunkt ist niedrig (steigt mit der Molekülgröße)
- Löslichkeit: schlecht in Stoffen, in denen starke Wasserstoffbrücken vorliegen
- Löslichkeit: schlecht in polaren Stoffen
- Alkane lösen keine Salze, da sie keine Solvationshüllen ausbilden
Alkane sind typisch unpolare Stoffe (hydrophob, wassermeidend).
Auf einen Blick – die wichtigsten Aussagen
REAKTIONSTRÄGHEIT
Starke, fast unpolare C–C- und C–H-Bindungen machen Alkane reaktionsträge – weder Säure noch Base noch Nucleophil noch Elektrophil.
ZMK
Zwischen Alkanmolekülen wirken nur van-der-Waals-Kräfte – keine Wasserstoffbrücken, keine Dipol-Wechselwirkungen.
SIEDEPUNKT
Mehr C-Atome → größere Moleküloberfläche → stärkere vdW-Kräfte → höherer Siedepunkt. Stärkere Verzweigung senkt den Siedepunkt.
HYDROPHOB
Alkane sind unpolar und wassermeidend (hydrophob). Sie lösen sich nicht in Wasser und lösen keine Salze.
Häufige Fragen – Eigenschaften der Alkane
Warum sind Alkane so reaktionsträge?
Die C–C- und C–H-Bindungen in Alkanen sind sehr stark und fast unpolar (Elektronegativitätsunterschied sehr gering). Dadurch bieten Alkane weder freie Elektronenpaare (kein Angriffspunkt für Elektrophile) noch eine Elektronenpaarlücke (kein Angriffspunkt für Nucleophile). Auch eine Protonenabgabe findet praktisch nicht statt. Nur unter extremen Bedingungen – sehr hohe Temperaturen oder UV-Licht – kommt es zur homolytischen Bindungsspaltung und damit zu einer radikalischen Reaktion.
Warum steigt der Siedepunkt der Alkane mit der Kettenlänge?
Mit jedem zusätzlichen C-Atom wächst die Moleküloberfläche. Größere Oberfläche bedeutet mehr Kontaktfläche zwischen den Molekülen und damit stärkere van-der-Waals-Kräfte. Um ein Molekül aus dem flüssigen Zustand zu befreien, muss mehr Energie aufgewendet werden → der Siedepunkt steigt. Methan (C1) siedet bei –162 °C, Hexan (C6) bereits bei +69 °C.
Warum lösen sich Alkane nicht in Wasser?
Wasser ist ein stark polares Lösungsmittel, das ausgeprägte Wasserstoffbrücken zwischen seinen Molekülen ausbildet. Alkane sind unpolar und können keine entsprechenden Wechselwirkungen mit Wasser eingehen. Nach dem Prinzip „Gleiches löst Gleiches" (lat. similia similibus solvantur) bleiben Alkane in Wasser ungelöst und bilden eine separate Phase (z. B. Öl auf Wasser). Salze lösen Alkane ebenfalls nicht auf, da Alkane keine Solvationshüllen um Ionen ausbilden können.
Warum haben verzweigte Alkane niedrigere Siedepunkte als unverzweigte?
Je stärker ein Alkan verzweigt ist, desto kompakter (kugelförmiger) ist das Molekül. Die Oberfläche, über die van-der-Waals-Kräfte wirken können, wird kleiner → die Anziehungskräfte zwischen den Molekülen sind schwächer → der Siedepunkt sinkt. Beispiel: n-Pentan (unverzweigt) siedet bei 36 °C, 2,2-Dimethylpropan (stark verzweigt) bereits bei 9 °C – obwohl beide die gleiche Summenformel C5H12 haben. Mehr dazu unter: → Isomere von C₇H₁₆.
Was ist die homolytische (radikalische) Spaltung einer Bindung?
Bei der homolytischen Spaltung teilen sich beide Bindungspartner die gemeinsamen Elektronen gleichmäßig auf – jedes Atom erhält ein Elektron. Es entstehen Radikale (Teilchen mit einem ungepaarten Elektron), die sehr reaktiv sind. Dies geschieht bei Alkanen nur unter extremen Bedingungen wie hohen Temperaturen oder UV-Strahlung. Es ist die Grundlage der radikalischen Substitution. Im Gegensatz dazu werden bei der heterolytischen Spaltung beide Elektronen von einem Partner behalten.
Lernkarten – Eigenschaften der Alkane
Klicke auf eine Karte, um die Antwort zu sehen.
1Warum sind Alkane reaktionsträge? Nenne zwei Gründe.
1. C–C- und C–H-Bindungen sind sehr stark.
2. Die Bindungen sind fast unpolar → kein Angriffspunkt für Nucleophile oder Elektrophile.2Welche ZMK wirken zwischen Alkanmolekülen?
Ausschließlich van-der-Waals-Kräfte. Keine Wasserstoffbrücken, keine Dipol-Dipol-Wechselwirkungen (Alkane sind unpolar).
3Warum steigt der Siedepunkt der Alkane mit der Kettenlänge?
Mehr C-Atome → größere Oberfläche → stärkere van-der-Waals-Kräfte → mehr Energie nötig zum Verdampfen → höherer Siedepunkt.
4Was bedeutet „hydrophob"? Warum sind Alkane hydrophob?
Hydrophob = wassermeidend. Alkane sind unpolar → können keine Wechselwirkungen mit polarem Wasser eingehen → lösen sich nicht in Wasser.
5n-Pentan oder 2,2-Dimethylpropan – welches hat den höheren Siedepunkt? Begründe.
n-Pentan (Sdp. 36 °C) > 2,2-Dimethylpropan (Sdp. 9 °C). n-Pentan ist gestreckter → größere Oberfläche → stärkere vdW-Kräfte – obwohl beide C5H12 sind.
Weiter im Kapitel Alkane
← 1.6 Übungen zur Nomenklatur → 1.8 Angriffsfreudige Teilchen
🔁 Grundlagen: Polare und unpolare Atombindung (Kl. 9) · Elektrische Dipole (Kl. 9)
