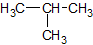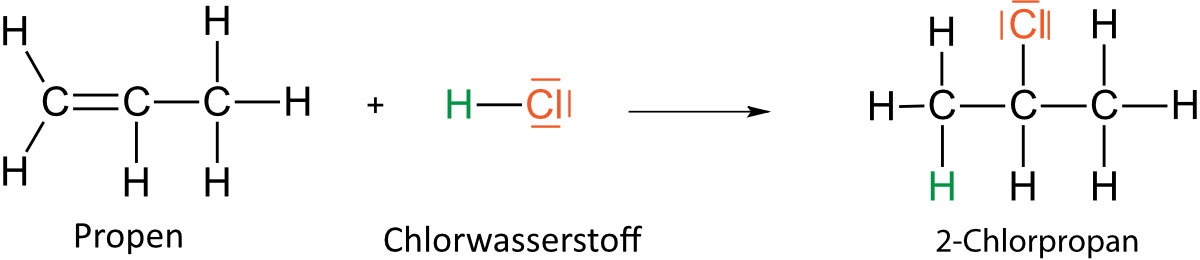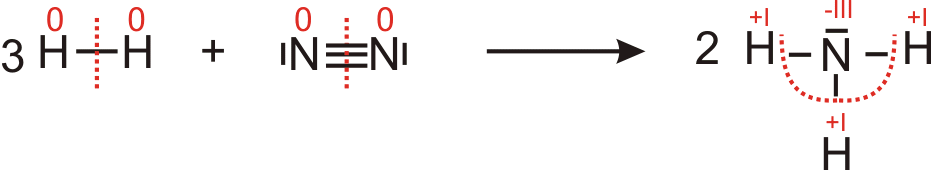Oxidationszahl
-
01.1 Methan
1. Alkane
1.1 Methan
1.1.1 Vorkommen:
im Erdgas, Sumpfgas, Biogas, Grubengas
1.1.2 Eigenschaften:
- farb- und geruchloses Gas
- geringere Dichte als Luft
- brennbar
1.1.3 Ermittlung der Summenformel (Molekülformel) und Strukturformel
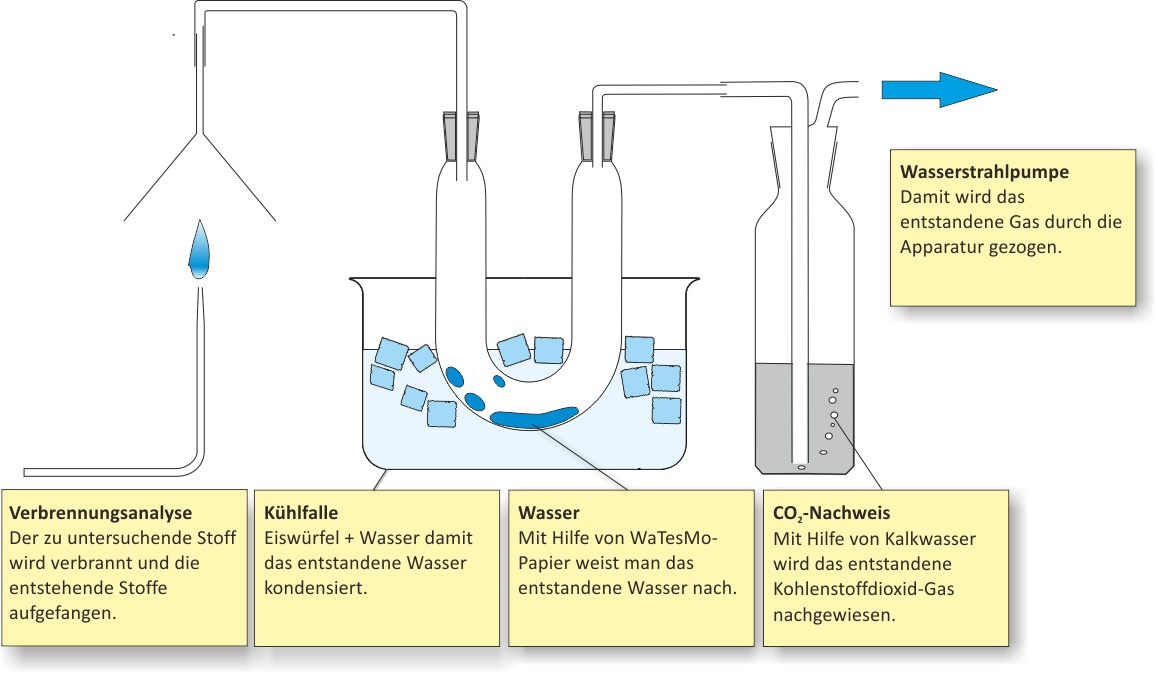
a) Qualitative Analyse (Elementaranalyse)
Hierfür wird der zu untersuchende Stoff verbrannt und die Verbrennungsprodukte werden bestimmt.
Bildet sich Wasser, wird Wasserstoff als Element vorhanden sein;
Kohlenstoff kann man einmal als Ruß (bei unvollständiger Verbrennung) oder als Kohlenstoffdioxid nachweisen. Der Kohlenstoffdioxid-Nachweis erfolgt mit der Kalkwasserprobe. Hierfür wird das entstandene Gas in Kalkwasser eingeleitet. Trübt sich die Lösung, ist Kohlenstoffdioxid vorhanden.- Nachweis von Wasserstoff → Bildung von Wasser → WaTesMo-Papier oder wasserfreies Kupfersulfat.
- Nachweis von C → Bildung von CO2 → Nachweis als CaCO3.
Ca(OH)2 (aq) + CO2 (g) → CaCO3 (s) + H2O (l)
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) ergeben, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält
b) Bestimmung der molaren Masse
Mit Hilfe der Gaswägung kann man die Molare Masse von Methan bestimmen: M(Methan) = 16 g/mol
Molekülmasse von Methan 16 u
c) Summenformel:
Daraus ergibt sich folgende Summenformel.
CH4
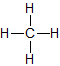
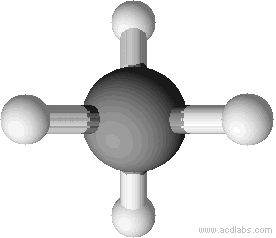
d) Strukturformel:Man zeichnet Methan meist mit einem Winkel von 90°. Dieser Winkel entspricht nicht dem Bindungswinkel (vgl. unten). Man kann sich aber vorstellen, dass man direkt auf das Molekül wie in der zweiten Abbildung dargestellt wird, blickt.
Tetraedrische Anordnung der Wasserstoffatome um das Kohlenstoffatom (Bindungswinkel 109,5 °).
Erklärung: Größtmögliche Entfernung der Wasserstoffatome.
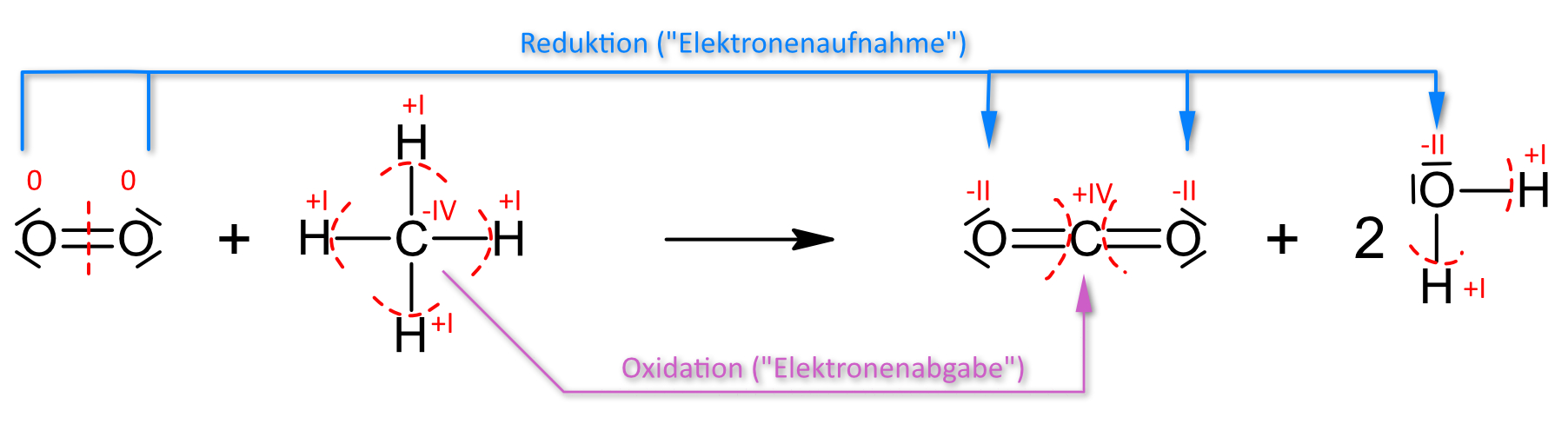
1.1.4 Vollständige Verbrennung:0 -IV +I +IV -II +I -II
2 O2 + CH4 → CO2 + 2 H2O ΔH = - 888 kJ/molHinweis: Wenn die Ermittlungs der Oxidationszahlen Schwierigkeiten macht, dann kann man es hier nochmals nachlesen.
1l Methan benötigt zur vollständigen Verbrennung 10 Liter Luft (2 l Sauerstoff). -
01.4 Butan
Hinweis: 1.2 Ethan und 1.3 Propan wird nur bei ausreichend Zeit und entsprechend vorrätigen Chemikalien als einzelne Punkte besprochen. Da es aber sowieso ähnlich ist, wird an dieser Stelle auf den Heftaufschrieb verzichtet (vgl. weiter unten: Homologe Reihe).
1.4 Butan
1.4.1 Vorkommen
im Erdgas, fällt an bei der Benzingewinnung
1.4.2 Eigenschaften
farbloses Gas, größere Dichte als Luft
brennbar (Verbrennungsprodukte bei vollständiger Verbrennung: CO2 und H2O )
unter Druck leicht verflüssigbar
1.4.3 Ermittlung der Summenformel (Molekülformel) und Strukturformela) Qualitative Analyse (Elementaranalyse)
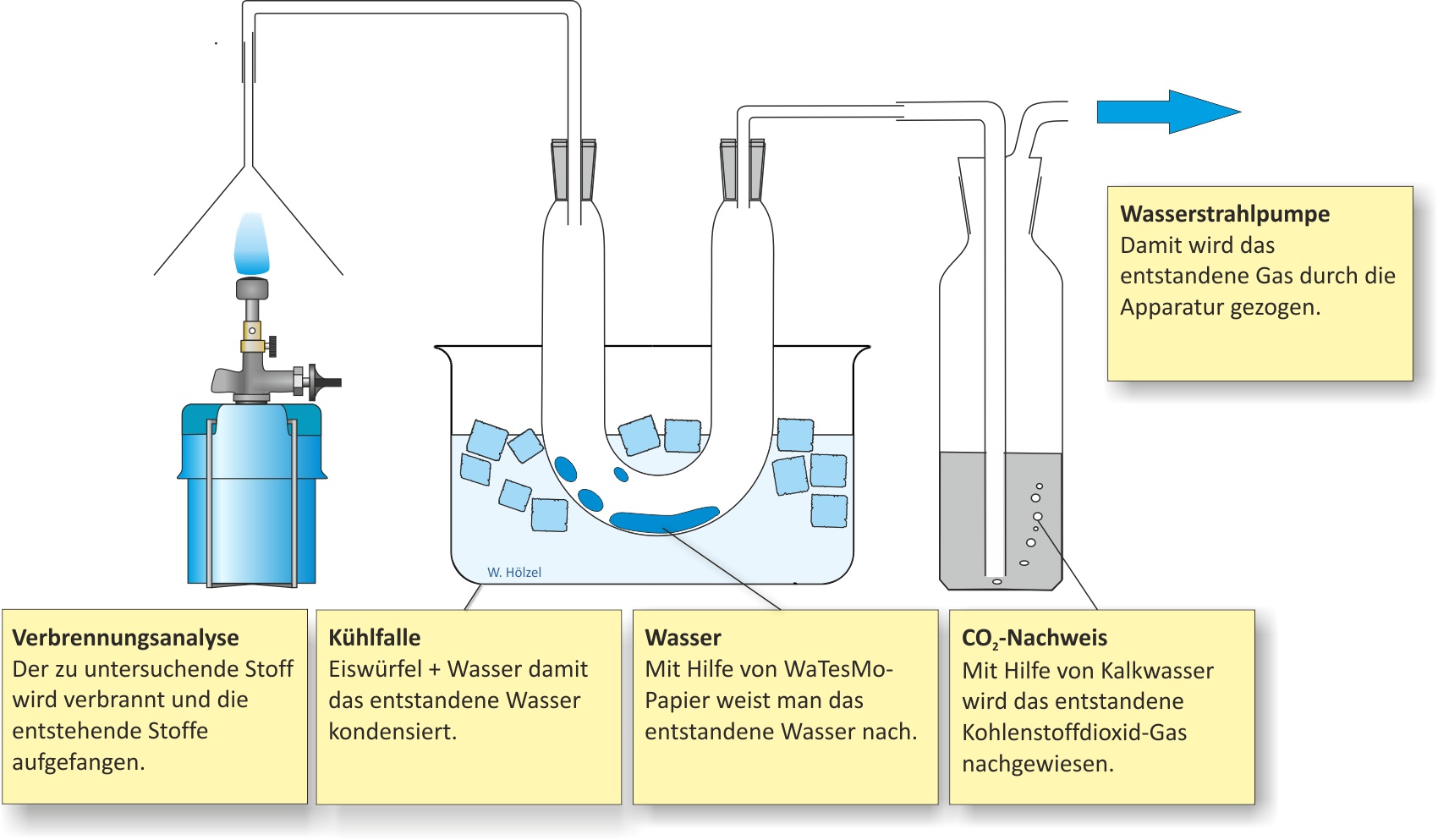
Die Verbrennungsprodukte (Wasser, Kohlenstoffdioxid) ergeben, dass Methan Kohlenstoff, Wasserstoff und eventuell Sauerstoff enthält
b) Bau und Formeln
1. Molare Masse = 58,12 g/mol
Molekülmasse = 58,12 u
2. Summenformel:C4H10
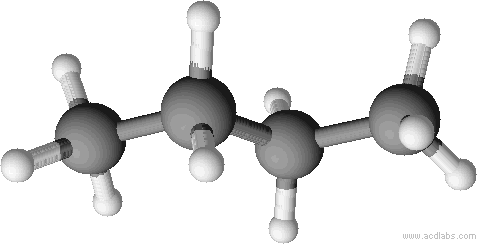
3. Strukturformel:
a) unverzweigte Kette b) verzweigte Kette
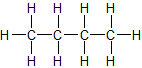

n-Butan Isobutan = 2-Methyl-Propan
Sdp.: - 0,5 °C Sdp.: - 12 °CZMK: nur van-der-Waals-Kräfte; bei n-Butan können sich die Moleküle dichter zusammenlagern und haben dadurch stärkere Zwischenmolekulare Kräfte, d.h. eine etwas höhere Siedetemperatur.
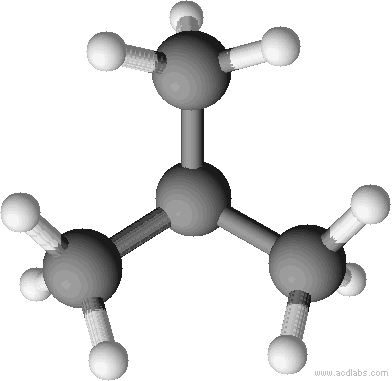
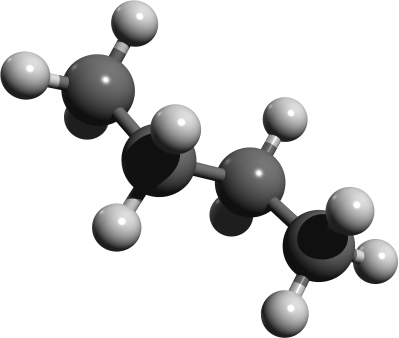
Räumliche Strukturen im Kugelstabmodell. Versucht die einzelnen Abbildungen Isobutan oder n-Butan zuzuordnen. Der Vorteil von Kugelstabmodelle sind, dass sie die Bindungen und Bindungswinkel anschaulich darstellen.
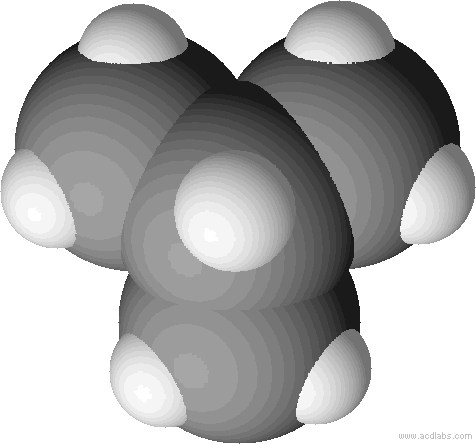
Kalottenmodell von 2-Methyl-Propan (= Isobutan). Bei Kalottenmodellen wird die Raumfüllung deutlich.
Da Strukturformeln bei größeren Molekülen zu lange dauern, hilft man sich mit der Halbstrukturformel aus, wobei die Wasserstoffatome quasi als Summenformel hinter das C geschrieben wird. Man schaut zunächst, wie viele Bindungen ein C schon hat und füllt dann mit so vielen H-Atomen auf, bis die Vierbindigkeit von Kohlenstoff erfüllt ist. Hier am Beispiel von Isobutan.
1.4.4 VerwendungHeizgas („blaue Gaskartuschen“), Kältemittel (Ersatz für FCKW), Treibgas in Sprays, Feuerzeuggas (häufig zusammen mit Propan)
1.4.5 Isomerie
(isos (griech.) = gleich; meros (griech.) = Teil)
Verbindungen, deren Moleküle bei gleicher Summenformel unterschiedliche Strukturformeln besitzen, bezeichnet man als Isomere. Isomere Verbindungen unterscheiden sich vor allem in ihren physikalischen Eigenschaften (Schmelz- und Siedepunkt) und wenig in ihren chemischen Reaktionen.
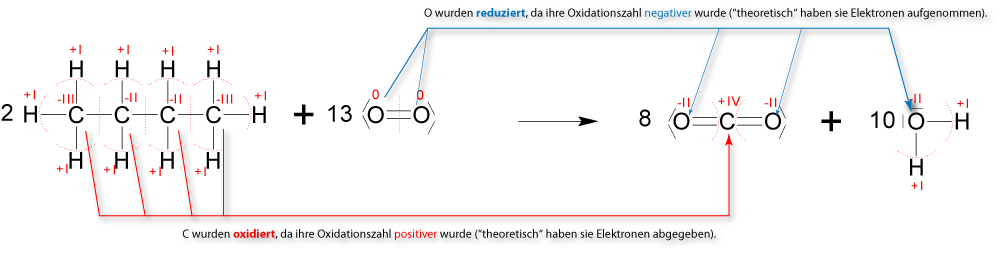
1.4.6 Vollständige Verbrennung (Oxidation)Wenn Butan vollständig verbrannt (oxidiert) wird, so entsteht dabei ausschließlich Kohlenstoffdioxid und Wasser.
-
1.4 Weitere Redoxreaktionen
1.4 Weitere (komplexere) Redoxreaktionen
Die Redoxreaktionen sind nicht immer ganz so einfach. Hier zunächst ein Beispiel:
Aufgabe: Schaut, welche Redox-Paare in eurer Tabelle (siehe Moodle) vorhanden sind.
Beispiel 1: Reaktion von Kaliumdichromat mit Eisen(II)-SulfatTeilchen: Kaliumdichromat: 2 K¹⁺ Cr₂O₇²⁻
Eisen(II)-sulfat: Fe²⁺ SO₄²⁻Oxidation: Fe²⁺ → Fe³⁺ + e⁻ | x 6
Reduktion: Cr₂O₇²⁻ + 14 H₃O⁺ + 6 e⁻ → 2 Cr³⁺ + 21 H₂ORedox: Cr₂O₇²⁻ + 14 H₃O⁺ + 6 Fe²⁺ → Fe³⁺ + 2 Cr³⁺ + 21 H₂O
Rktgl: 6 FeSO₄ (aq) + K₂Cr₂O₇ (aq) + 7 H₂SO₄ (aq) → 3 Fe₂(SO₄)₃ (aq) + Cr₂(SO₄)₃ (aq) + K₂SO₄ (aq) + 7 H₂O (l)
Beispiel 2: „Cl-Gas kann im Labor gewonnen werden, indem man Kaliumdichromat mit Salzsäure reagieren lässt. Der Ansatz für die Reaktionsgleichung lautet:
__ Cr₂O₇²⁻ + __H₃O⁺ + __ Cl⁻ → ___Cr³⁺ + __Cl₂ + __ H₂ORichten Sie die Redoxgleichung ein. Formulieren Sie dazu die Teilgleichungen mit Oxidationszahlen.
{slider title="Lösung" open="false" class="icon"}
Oxidation: 2 Cl⁻ → Cl₂ + 2 e⁻ | x 3
Reduktion: Cr₂O₇²⁻ + 14 H₃O⁺ + 6 e⁻ → 2 Cr³⁺ + 21 H₂O
Redox: Cr₂O₇²⁻ + 14 H₃O⁺ + 6 Cl⁻ → 3 Cl₂ + 2 Cr³⁺ + 21 H₂O{/sliders}
Aufgabe 1: Geben Sie in den nachfolgenden Formeln die Oxidationszahlen aller Atome an:
(vgl. Tafelanschrieb)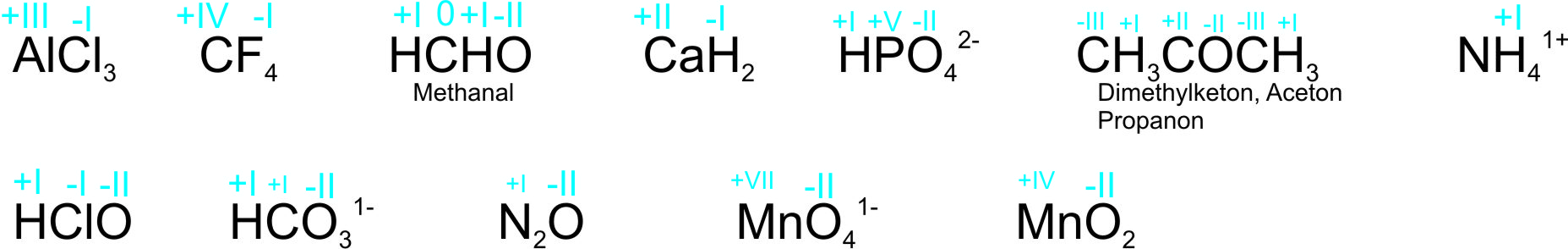
Aufgabe 2: Auf konzentrierte Kaliumpermangantlösung (KMnO₄) lässt man konzentrierte Salzsäure (HCl) einwirken. Bei dieser Reaktion entsteht u.a. Chlorgas und Mangan(II)-chlorid.
Vervollständigen Sie die folgenden Gleichungen für die obige Redoxreaktion (Vereinfacht wird statt H₃O⁺ H⁺ formuliert).{slider title="Tipp" open="false" class="icon"}
__ Cl⁻ + __ MnO₄¹⁻ + __ H⁺ → __ Cl₂ + __ Mn²⁺ + __ H₂O
{/sliders}
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
2.3 Katalytische Hydrierung
2.3 Katalytische Hydrierung
Hinweis: Markownikow-Regel: Bei Addition von z.B. Halogenwasserstoff bekommt das wasserstoffhaltigere C-Atom bekommt das H; das wasserstoffärmere Atom bekommt dann das Halogen. "Wer hat, dem wird gegeben" [bezieht sich auf H-Atome].
a) Alle Alkene lassen sich zu Alkane hydrieren.Hierbei handelt es sich um eine Redoxreaktion! Kohlenstoff wird reduziert (Oxidationszahlerniedrigung), H wird oxidiert. Hydrierung: Reduktion von Kohlenstoff
Die Dehydrierung ist die Umkehrung der Hydrierung: Oxidation von Kohlenstoff
b) Allgemein: Die Hydrierung ist eine umkehrbare Reaktion (Dehydrierung)
Eliminierungsreaktionen: Abspaltung kleiner Moleküle!
Übungsaufgabe:
An Propen wird Chlorwasserstoff addiert. Formuliere hierfür eine Reaktionsgleichung in Strukturformeln mit bindenden und nichtbindenden Elektronenpaaren. Beachte dabei auch die Markownikow-Regel (siehe oben).
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
3 Redoxreaktionen mit Molekülen - Oxidationszahlen
3 Redoxreaktionen mit Molekülen
Bei der Verbrennung von Stoffen bilden sich Oxide, ohne dass es zur Bildung von Ionen kommt. Beispiele dafür sind die Verbrennung von Wasserstoff, Kohlenstoff, Schwefel und Phosphor.
Um diese Reaktion als Redoxreaktion erfassen zu können, hat man als Hilfsgröße die Oxidationszahl eingeführt.
3.1 Oxidationszahl
Def.: Die Oxidationszahl gibt an, welche Ladung ein Atom in einem Molekül oder in einem anderen Teilchen hätte, wenn alle am Aufbau des Teilchens beteiligten Atome in Form von Ionen vorlägen.
Die sich für die Atome in der Verbindung ergebenden formalen Ladungszahlen nennt man Oxidationszahlen. Zur Unterscheidung von Ionenladungen werden sie als römische Zahlen an die Elementsymbole geschrieben.
Vorgehensweise: Vgl. dazu die zwei Beispiele 3.2 und 3.3 um die Schritte nachvollziehen zu können.
1. Schritt: Strukturformel erstellen.
2. Schritt: Ermittlung der Elektronegativität aller Elemente (siehe PSE) :
3. Schritt: Bindungselektronen werden formal dem elektronegativeren Bindungspartner zugeteilt. Besitzen die Bindungspartner die gleiche Elektronegativität erhalten sie je die Hälfte der Bindungselektronen.Faustregel: (Hinweis: Wann immer eindeutige Strukturformeln möglich sind, würde ich keine Faustregeln nutzen)
- Fluor immer: –I
- Wasserstoff: +I
- Sauerstoff: -II
- Halogene: -I (sofern nicht mit Sauerstoff oder einem elektronegativeren Halogen verbunden sind)
4. Schritt: Man bestimmt die Hauptgruppennummer des Elements und zählt dann die Elektronen, welche das Element jetzt "formal" hätte (vgl. 3. Schritt). Dann berechnet man entsprechend folgender Formel:
Oxidationszahl = Hauptgruppennummer des Elements – Elektronenanzahl im Molekül
Bsp. Sauerstoff im Wassermolekül: Oxidationszahl(O) = steht in der 6. Hauptgruppe = VI - 8 = -2 (bzw. - II)
Bsp. Wasserstoff im Wassermolekül: Oxidationszahl(H) = I - 0 = +1
5. Schritt: Kontrolle: Summe der Oxidationszahlen muss 0 sein (bei elektr. Neutralen Molekülen).
Mit Hilfe der Oxidationszahl lassen sich die Begriffe Oxidation und Reduktion neu fassen:Oxidation: Elektronenabgabe) bedeutet eine Erhöhung der Oxidationszahl.
Reduktion: (Elektronenaufnahme) bedeutet eine Erniedrigung der Oxidationszahl.
Redoxreaktionen: sind Vorgänge bei denen sich die Oxidationszahlen der beteiligten Atomarten ändern.3.2 Vollständige Verbrennung von Kohlenstoff
Kohlenstoff Sauerstoff Kohlenstoff(IV)-oxid
Atom Molekül Molekül

→ Kohlenstoff wird oxidiert, Sauerstoff wird reduziert.3.3 Reaktion von Wasserstoff mit Sauerstoff
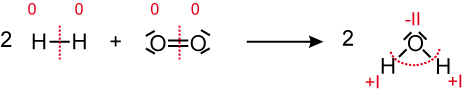
Wasserstoff Sauerstoff Wasser
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wird oxidiert
Oxidationszahlen von Sauerstoff wird negativer → Sauerstoff wird reduziert3.5 Reaktion von Wasserstoff mit Stickstoff zu Ammoniak (Ammoniaksynthese)
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
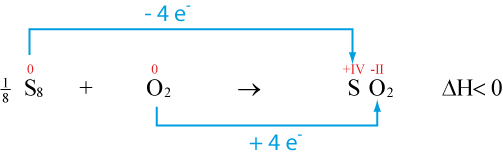
Oxidationszahlen von Stickestoff wurde negativer → Stickstoff wurde reduziert3.6 Reaktion von Schwefel mit Sauerstoff zu Schwefeldioxid
Man muss nicht immer die Lewis-Formeln (Strukturformeln) zeichnen. Manchmal genügt es, nach den Faustregeln zu arbeiten.
Oxidationszahlen von Schwefel wird positiver → Schwefel wurde oxidiert
Oxidationszahlen von Sauerstoff wurde negativer → Sauerstoff wurde reduziert3.7 Synthese von Chlorwasserstoff aus den Elementen
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Chor wurde negativer → Chlor wurde reduziert3.8 Synthese von Schwefelwasserstoff aus den Elementen
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Schwefel wurde negativer → Schwefel wurde reduziert -
6.1.4 Aldehydnachweise
6.1.4 Aldehydnachweise
a) Schiffsche-Probe mit Fuchsinschwefliger Säure
Fuchsinschweflige Säure ergibt mit Aldehyden eine rotviolette Farbe. Dieser Aldehydnachweis beruht nicht auf der Reduktionswirkung von Aldehyden!
b) Tollens-Probe (Silberspiegel)
Versuchsaufbau (gilt auch für Fehling-Probe)
Versuchsdurchführung:
Schutzbrille aufsetzen, weite Ärmel hochkrempeln, Haare zurückbinden.
- Gib in das RG etwa zwei fingerbreit Silbernitratlösung.
- Füge mit der Pipette tropfenweise verdünnte Ammoniaklösung hinzu, bis sich der entstehende Niederschlag gerade wieder auflöst.
- Gib nun in das RG zwei fingerbreit Probelösung.
- Stelle das RG in das heiße Wasserbad.
Beobachtung:
Es bildet sich ein Silberspiegel auf der Innenseite des Reagenzglas.
Auswertung:
Es bedeutet, dass sich die Silber-Ionen zu elementarem Silber reduzierthaben. Da eine Reduktion nur zusammen mit einer Oxidationablaufen, muss etwas anderes oxidiert worden sein. Da es ein Aldehyd-Nachweisist, kann man davon ausgehen, dass das C-Atom der Aldehyd-Gruppe oxidiertwurde. Da diese Reaktion in alkalischer Lösung abläuft (Ammoniak wurde dazugegeben), formuliert man mit Hilfe von Hydroxid-Ionen (OH⁻).
c) Fehling-Reagenz
Versuchsdurchführung:
Schutzbrille aufsetzen, weite Ärmel hochkrempeln, Haare zurückbinden.- Gib in das RG etwa 5 ml Fehling 1-Lösung und dann 5 ml Fehling 2-Lösung.
- Füge ein Spatellöffel Glucose zu.
- Stelle das RG nach kurzem Schütteln in das heiße Wasserbad.
Beobachtung:
Es bildet sich ein roter Niederschlag von Kupfer(I)-Oxid (Cu₂O).Auswertung:
Diese Reaktion verläuft recht analog zum Silberspiegel (Tollens-Reagens). Nur wird hierbei das Metall-Ion nicht komplett reduziert, sondern das Cu²⁺ wird zu Cu¹⁺ reduziert, wobei es sich sofort mit einem Oxid-Ion verbindet und den rötlichen Niederschlag bildet. Sauerstofflieferant ist auch in diesem Fall wie bei Tollens-Probe das Hydroxid-Ionen, da eine alkalische Lösung vorliegt.
Aufgabe: Versucht mit Hilfe der oberen Gleichung jetzt die Reaktionsgleichungen für das Fehlingreagenz zu formulieren.
{slider title="Lösung" open="false" class="icon"}
{/sliders}