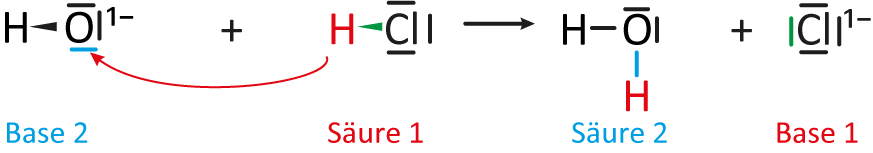Natriumhydroxid
-
3 Reaktion von festem Ammoniumchlorid und festem Natriumhydroxid
3 Reaktion von festem Ammoniumchlorid und festem Natriumhydroxid
a) Versuch mit Skizze
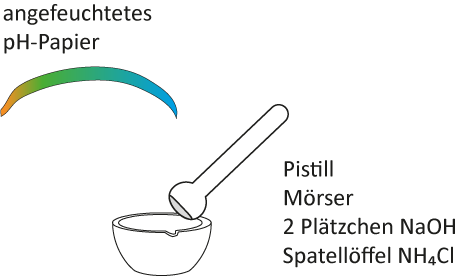
Die beiden Salze NH₄Cl und NaOH werden gemeinsam im Mörser zerrieben. Nach dem Zerreiben wird ein angefeuchtetes Indikatorpapier über die Schale gehalten; zusätzlich wird eine Geruchsprobe vorgenommen.
b) Beobachtung:Es entsteht ein stechend riechendes Gas. Das feuchte Indikatorpapier färbt sich blau. Die Festsubstanz im Mörser wird feucht.
c) Auswertung:
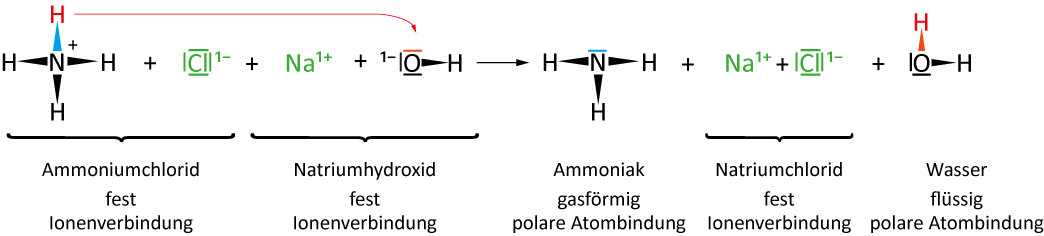
I. Teilchengleichung
II. ReaktionsgleichungNH₄Cl + NaOH → NH₃ + NaCl + H₂O Ammoniumchlorid Natriumhydroxid Ammoniak Natriumchlorid Wasser III. Protolysenschema
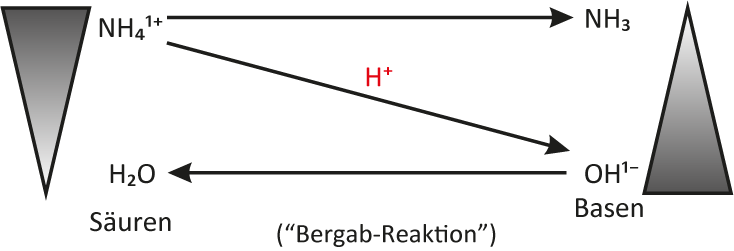
Aufgabe: Formuliert für diese chemische Reaktion ein Protolyse-Schema
{slider title="Lösung: Protolyse-Schema für das Verreiben von Ammoniumchlorid und Natriumhydroxid" open="false" class="icon"}
{/sliders}
-
Säure-Base-Reaktionen (Protolysen)
Säure-Base-Reaktionen (=Protolyse-Reaktionen)
In diesem Kapitel geht es um die zweite Möglichkeit, wie eine chemische Reaktion ablaufen kann. Dabei werden zunächst einige typische Beispiele betrachtet. Danach wird die Definition (die bis dahin sowieso wohl schon vielen klar sein wird) aufgestellt.
1 Reaktion von Chlorwasserstoffgas mit festem Natriumhydroxid
Hinweis: Um die Vorgänge besser nachvollziehen zu können gibt es hier ein Periodensystem der Elemente-Popup
Ausgangsstoffe:
Name Summenformel Strukturformel Bindung Chlorwasserstoff HCl 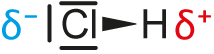
Polare Atombindung Natriumhydroxid NaOH Ionenbindung a) Versuch:
Abb.: Herstellung von HCl und anschließende Reaktion mit NaOH
b) Beobachtung:
Natriumhydroxid überzieht sich mit einem weißen Feststoff; am Ende des Glasrohres schlägt sich eine farblose Flüssigkeit nieder, das Reaktionsrohr erwärmt sich.
c) Auswertung: Folgende Teilchen reagieren miteinander:
I Teilchengleichung:Na¹⁺OH¹⁻ + HCl → H₂O + Na¹⁺Cl¹⁻
NaOH(s) + HCl(g) → H₂O(l) + NaCl(s) ΔH < 0
d) Protolyse-Schema
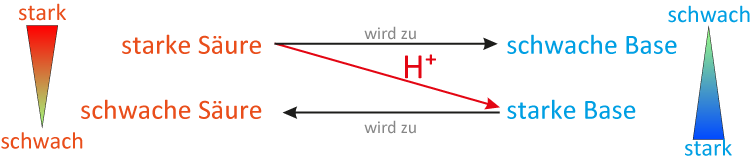
Allgemeines Protolyse-SchemaEin Protolyse-Schema funktioniert analog zum Redox-Schema (siehe vorheriges Kapitel). Hier zunächst ein allgemeines Schema (welches für alle Säure-Base-Reaktion so gelten kann):
Protolyse-Sschema für die Bildung von Natriumchlorid
e) Erklärung der exothermen Reaktion
ΔH > 0 (positiv, endotherm) ΔH < 0 (negativ, exotherm) - Deprotonierung von Chlorwasserstoff
- Gitterspaltung von Natriumhydroxid
- Protonierung des Hydroxid-Ions
- Gitterbildung von Natriumchlorid
- wasserstoffbrückenbildung zwischen verschiedenen H₂O-Molekülen
Ergebnis: ΔH < 0 (negativ, exotherm) überwiegt.