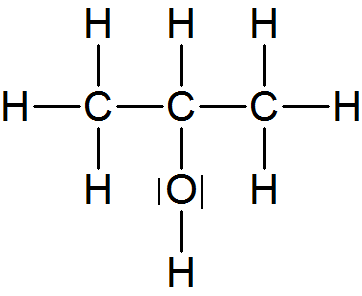
Ethanol
-
2.6 Phenole
2.6 Phenole = Hydroxybenzole
Vorkommen:
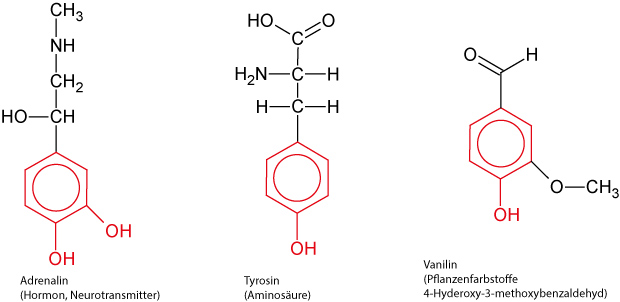
2.6.1 Monohydroxybenzol = Phenol
a) Physikalische Eigenschaften
- Smp.: 40,9; Sdp.: 181,9 °C
- In Wasser nur mäßig löslich (bildet bei ZT eine Emulsion)
- Starkes Zellgift, durch Haut resorbiert
b) Chemische Eigenschaften
- Oxidiert an Luft leicht ⇨ rötliche Färbung
- Karbolsäure“: 2 %ige Säure; Desinfektion
- Im Gegensatz zu Ethanol sauer:
1. Phenol als schwache Säure
pKS = 9,95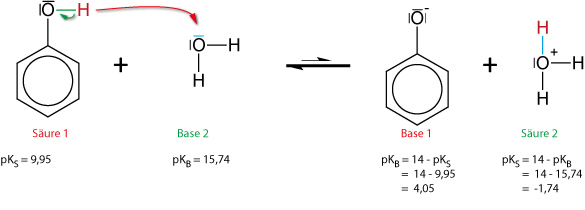
Grenzformeln des Phenolations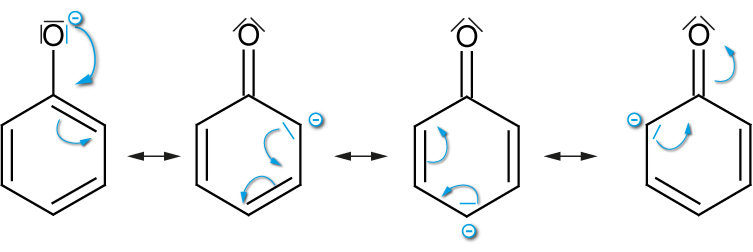
Phenol Ethanol Säurestärke höher niedriger Induktiver Effekt 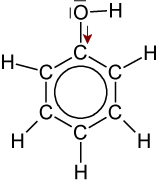
schwacher -I-Effekt ⇨ elektronenziehend
⇨ H⁺-Abgabe ist erleichtert
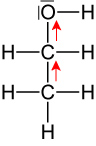
+I-Effekt ⇨ Elektro-nenschiebend
H⁺-Abgabe ist er-schwert.Anion: Mesomeriestabilisiert konjungierte Base (Phenolat): negative Ladung ist über den ganzen Ring delokalisiert ⇨ stabilisiert! Keine Stabilisierung durch Mesomerien Brønsted-Säure stärker schwächer Brønsted-Base schwächer stärker 2.6.3 Synthese
90% der Weltproduktion nach der Hock-Synthese
Wirtschaftliches Verfahren, da auch Aceton nutzbar ist.
siehe Heftaufschrieb
2.6.4 Verwendung
Herstellung von Kunststoffen (Polyamide, Phenoplasten, Phenolharzen und Polycarbonaten)
-
5 Alkanol, Alkohol
5 Alkanol, Alkohol
5.1 Ethanol, Trinkalkohol, Weingeist
5.1.1 Herstellung
Alkoholische Gärung:
Mikroorganismen (z.B. Hefe = Pilze) nutzen diesen Stoffwechselweg zur Energiegewinnung, wenn kein Sauerstoff vorhanden ist (= anaerobe Bedingungen). Dabei werden Kohlenhydrate (vor allem Glucose) mit Hilfe von Enzymen (Biokatalysatoren) in Kohlenstoffdioxid und Ethanol umgewandelt.Zucker (Glucose) --(Hefe)--> Ethanol + Kohlenstoffdioxid ΔH < 0
Ferner entstehen Glycerin, Methanol, „Fuselalkohole“ (= höhere Alkohole), Aldehyde, Ketone, organische Säuren und Ester.
Bei einem Volumenanteil von etwa 14% Ethanol stellen die meisten Hefen ihre Tätigkeit ein.
Problem: Wie kann höher konzentriertes Ethanol gewonnen werden?
Lösung:
Destillation: Ein Verfahren zur Trennung von Flüssigkeitsgemischen durch Verdampfen und anschließender Kondensation des Dampfes.Vgl. AB .
5.1.2 Eigenschaften
a) physikalische
- farblose Flüssigkeit
- Siedetemperatur: +78°C
- Schmelztemperatur: -114°C
- Gute Mischbarkeit mit Wasser und Benzin (SE )
b) chemische
- brennbar
-
5 Alkohole - Alkanole
Was du in diesem Kapitel lernst
Alkohole (Alkanole) sind Kohlenwasserstoffe mit mindestens einer OH-Gruppe (Hydroxygruppe). Am Beispiel des Ethanols lernst du Eigenschaften, Formelermittlung und typische Reaktionen kennen. Dazu kommen die homologe Reihe, der induktive Effekt und die wichtigen mehrwertigen Alkohole wie Glycerin und Glykol.
Grundlagen aus der 10. Klasse
Alkohole enthalten eine C-Kette wie die Alkane, Alkene und Alkine. Wiederhole bei Bedarf: → 3. Alkine – C≡C-Dreifachbindung, Additionsreaktion · → 2. Alkene – Funktionelle Gruppen, Isomerie
Kapitelübersicht – 5. Alkohole (Alkanole)
Klicke auf eine Kachel, um direkt zum Unterkapitel zu springen.
5.1 Ethanol
C₂H₅OH5.1
Ethanol
Herstellung · Physikalische & chemische Eigenschaften · Alkoholismus
→ 5.1.1 Herstellung · 5.1.2 Eigenschaften · 5.1.6 Alkoholismus5.1.3
Formelermittlung
Verbrennungsanalyse · Summen- und Strukturformel von Ethanol · Molare Masse
5.1.4
Ethanol + Alkalimetall
Versuch: Natrium in Ethanol · Reaktionsgleichung · Vergleich mit Wasser
5.1.5
Induktiver Effekt
+I-Effekt und −I-Effekt · Elektronenverschiebung · Polarität der O–H-Bindung
5.2 Homologe Reihe & Systematik
5.2
Homologe Reihe der Alkohole
Hydroxy- & Methylgruppe · wichtige Alkohole · Löslichkeit · H-Brückenbindung
→ 5.2.1 Gruppen · 5.2.2 Wichtige Alkohole · 5.2.3 Löslichkeit5.2.4 / 5.2.5
Primär · Sekundär · Tertiär
Unterscheidung nach C-Nachbarn · allgemeine Formel der Alkanole CnH2n+1OH
5.2.6
Mehrwertige Alkohole
Glykol (Ethandiol) · Glycerin (Propantriol) · Sorbit · Vorkommen & Verwendung
5.3 Reaktionen · 5.4 Ether
5.3
Chemische Reaktionen
Bindungsverhältnisse · Redox mit Na · Verbrennung · Reaktion mit HBr · Dehydratisierung
→ 5.3.1–5.3.5 am Beispiel von Ethanol5.4
Ether
Herstellung · Physikalische Eigenschaften · Chemische Eigenschaften · Verwendung
⚠️ Seite noch nicht online
Auf einen Blick – die wichtigsten Aussagen
Funktionelle Gruppe
Alkohole besitzen eine oder mehrere OH-Gruppen (Hydroxygruppen). Die Formel einwertiger Alkanole lautet CnH2n+1OH. Die OH-Gruppe bestimmt die typischen Eigenschaften: Löslichkeit in Wasser, H-Brückenbindungen, Reaktivität.
Induktiver Effekt
Der negative induktive Effekt (−I) des Sauerstoffs zieht Elektronen aus der C–O-Bindung, wodurch das H in der OH-Gruppe leicht abspaltbar (schwach sauer) wird. Alkylgruppen zeigen den +I-Effekt.
prim / sek / tert
Primäre Alkohole: OH am C-Atom mit 1 C-Nachbarn. Sekundäre: 2 C-Nachbarn. Tertiäre: 3 C-Nachbarn. Die Klassifizierung bestimmt das Reaktionsverhalten (z. B. Oxidierbarkeit).
Reaktionen
Ethanol reagiert als schwache Säure mit Natrium (→ Natriumethanolat + H2), verbrennt zu CO2 + H2O und reagiert mit HBr durch nucleophile Substitution zu Bromoethan.
Häufige Fragen – Alkohole (Alkanole)
Was sind Alkohole, und was ist ihre funktionelle Gruppe?
Alkohole (Alkanole) sind organische Verbindungen mit mindestens einer Hydroxygruppe (–OH). Das einfachste Mitglied ist Methanol (CH3OH), das wichtigste im Alltag ist Ethanol (C2H5OH). Die allgemeine Formel einwertiger Alkanole lautet CnH2n+1OH. Die OH-Gruppe verleiht Alkoholen ihre charakteristischen Eigenschaften: gute Wasserlöslichkeit (durch H-Brücken), höhere Siedepunkte als vergleichbare Alkane, und schwach saures Verhalten gegenüber Alkalimetallen.
Was unterscheidet primäre, sekundäre und tertiäre Alkohole?
Die Klassifizierung richtet sich danach, an wie vielen C-Atomen das OH-tragende Kohlenstoffatom gebunden ist: Primärer Alkohol: das OH-C hat einen C-Nachbarn (z. B. Ethanol, 1-Propanol). Sekundärer Alkohol: das OH-C hat zwei C-Nachbarn (z. B. 2-Propanol = Isopropanol). Tertiärer Alkohol: das OH-C hat drei C-Nachbarn (z. B. 2-Methyl-2-propanol). Diese Unterscheidung ist entscheidend für die Oxidierbarkeit: primäre → Aldehyde → Carbonsäuren; sekundäre → Ketone; tertiäre können nicht oxidiert werden. → 5.2.4
Wie reagiert Ethanol mit Natrium, und was beweist das über die OH-Gruppe?
Ethanol reagiert mit Natrium ähnlich wie Wasser, jedoch langsamer: 2 C2H5OH + 2 Na → 2 C2H5ONa + H2↑. Es entsteht Natriumethanolat und Wasserstoffgas. Die Reaktion zeigt, dass die OH-Gruppe in Alkoholen schwach sauer ist: das H-Atom der OH-Gruppe wird als H⁺ abgegeben (schwächere Säure als Wasser, weil der +I-Effekt der Ethylgruppe die O–H-Bindung weniger polarisiert). → 5.1.4
Was ist der induktive Effekt, und wie wirkt er in der OH-Gruppe?
Als induktiven Effekt bezeichnet man die Verschiebung der Elektronendichte in einer Bindungskette durch einen elektronegativen oder elektropositiven Substituenten. Der Sauerstoff der OH-Gruppe ist stark elektronegativ und zieht Elektronen aus dem benachbarten C-Atom heraus → negativer induktiver Effekt (−I). Die O–H-Bindung ist stark polarisiert, das H-Atom leicht abspaltbar. Alkylgruppen geben Elektronen ab (+I-Effekt), was die Säurestärke der Alkohole gegenüber Wasser leicht herabsetzt. → 5.1.5
Was sind mehrwertige Alkohole, und wo kommen sie vor?
Mehrwertige Alkohole tragen mehr als eine OH-Gruppe. Wichtige Vertreter: Glykol (Ethan-1,2-diol, 2 OH-Gruppen) – Frostschutzmittel und Ausgangsstoff für Kunststoffe (PET). Glycerin (Propan-1,2,3-triol, 3 OH-Gruppen) – natürlicher Bestandteil von Fetten und Ölen, Zusatz in Kosmetik, Lebensmitteln und Arzneimitteln. Sorbit (Hexan-1,2,3,4,5,6-hexol) – Zuckerersatzstoff. Durch die vielen OH-Gruppen bilden mehrwertige Alkohole besonders viele H-Brücken → sehr hohe Siedepunkte, sirupartige Konsistenz. → 5.2.6
Lernkarten – Alkohole
Klicke auf eine Karte, um die Antwort zu sehen.
1Was ist die funktionelle Gruppe der Alkohole? Wie lautet die allgemeine Formel?
Funktionelle Gruppe: –OH (Hydroxygruppe)
Allgemeine Formel einwertiger Alkanole: CnH2n+1OH
Beispiele: Methanol CH3OH · Ethanol C2H5OH2Was ist ein primärer, sekundärer und tertiärer Alkohol? Nenne je ein Beispiel.
Primär: OH-C hat 1 C-Nachbarn → Ethanol
Sekundär: 2 C-Nachbarn → 2-Propanol
Tertiär: 3 C-Nachbarn → 2-Methyl-2-propanol
Tertiäre Alkohole sind nicht oxidierbar.3Was passiert, wenn Ethanol mit Natrium reagiert? Gleichung?
2 C2H5OH + 2 Na →
2 C2H5ONa + H2↑
Natriumethanolat + Wasserstoff. Langsamer als Na + H₂O (schwächere Säure).4Was ist Glycerin? Nenne Formel, Anzahl der OH-Gruppen und eine Verwendung.
Propan-1,2,3-triol
Formel: C3H5(OH)3
3 OH-Gruppen → sirupartig, hygroskopisch
Verwendung: Kosmetik, Lebensmittel (E422), Fettbaustein5Berechne: Wie viel g H2 entstehen bei der Reaktion von 46 g Ethanol mit überschüssigem Natrium?
2 C2H5OH + 2 Na → 2 C2H5ONa + H2
M(C2H5OH) = 46 g/mol → n = 1 mol
Verhältnis 2:1 → n(H2) = 0,5 mol
m(H2) = 0,5 · 2 g/mol = 1 g H2
Weiter im Fach Chemie / 10. Klasse
← 3. Alkine → 6. Carbonylverbindungen ↑ Übersicht 10. Klasse
🔭 Vertiefung in der Kursstufe: Naturstoffe – Aminosäuren, Glucose, Enzyme
-
5.1.3 Formelermittlung von Ethanol
5.1.3 Formelermittlung von Ethanol
I. Qualitative Elementaranalyse
Versuch 1: Verbrennungsanalyse
- Ethanol verbrennt zu Wasser und Kohlenstoffdioxid;
- Nachweis von CO₂: Kalkwasser (weißer NS)
- Nachweis von H₂O: Watesmo-Papier wird blau
1. Ergebnis: Ethanol enthält somit zumindest C und H.
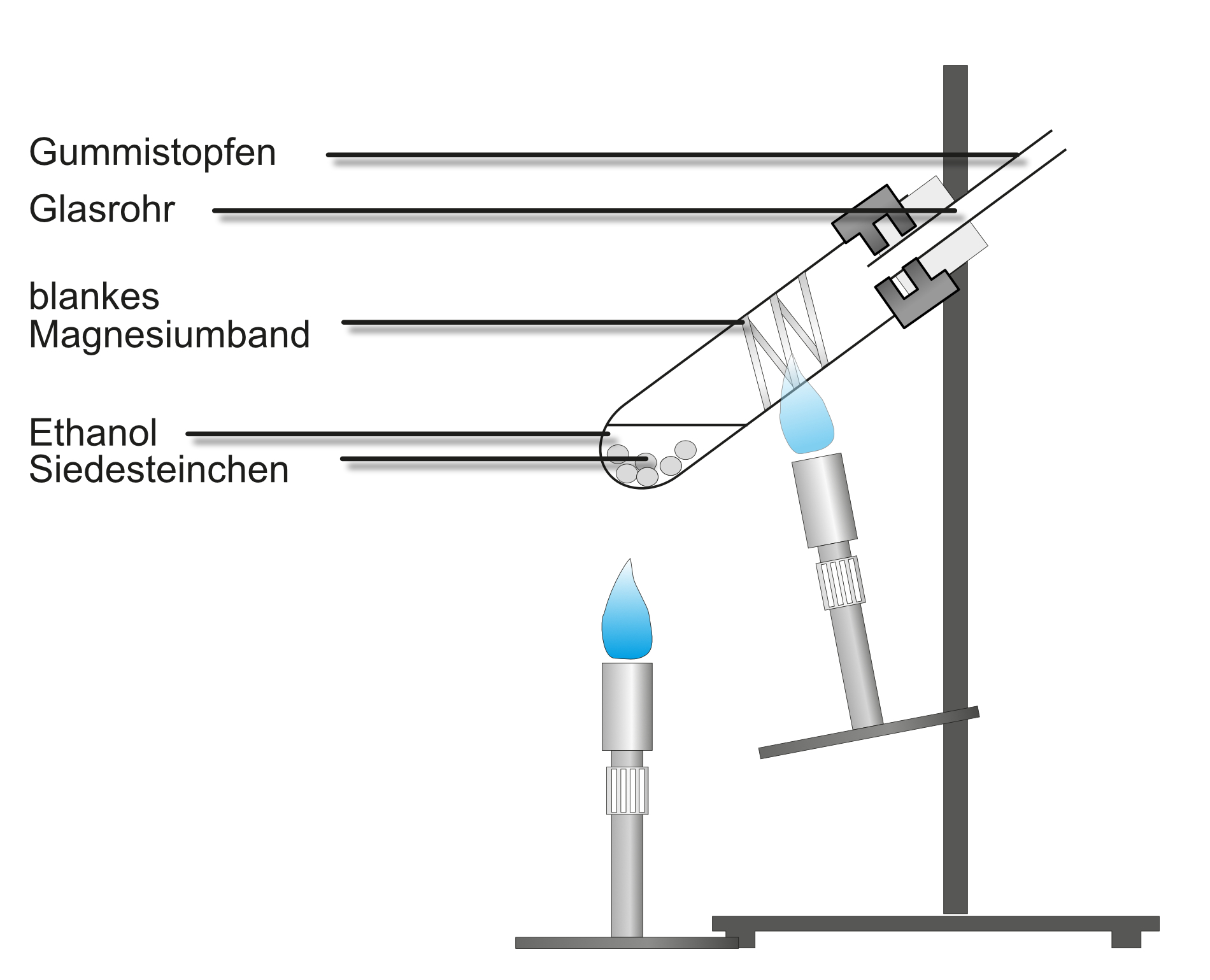
Versuch 2: Ethanol reagiert mit Magnesium - SauerstoffnachweisDurchführung:
- Aufbau siehe Abbildung
- Zunächst wird das Magnesiumband zum Glühen gebracht
- Danach verdampft man den Alkohol, der über das glühende Magnesiumband streicht.
Beobachtung:
Sobald Ethanol über das glühende Magnesiumband streicht glüht dieses heller auf und es bleibt ein kristalliner weißer Feststoff (Magnesiumoxid) übrig.
Ergebnis:
- Ethanol enthält neben Kohlenwasserstoff und Wasserstoff noch Sauerstoff.
II. Molekülmassenbestimmung (Verdampfungsmethode)
Hinweis: Dieser Versuch nur bei ausreichender Zeit durchgeführt. Nicht wundern, falls ihr das nicht im Heft stehen habt (dann kommt es auch in der Klausur nicht dran).
{slider title="Molmassenbestimmung nur bei viel Zeit" open="false" class="icon"}
Versuch: Molmassenbestimmung von Ethanol
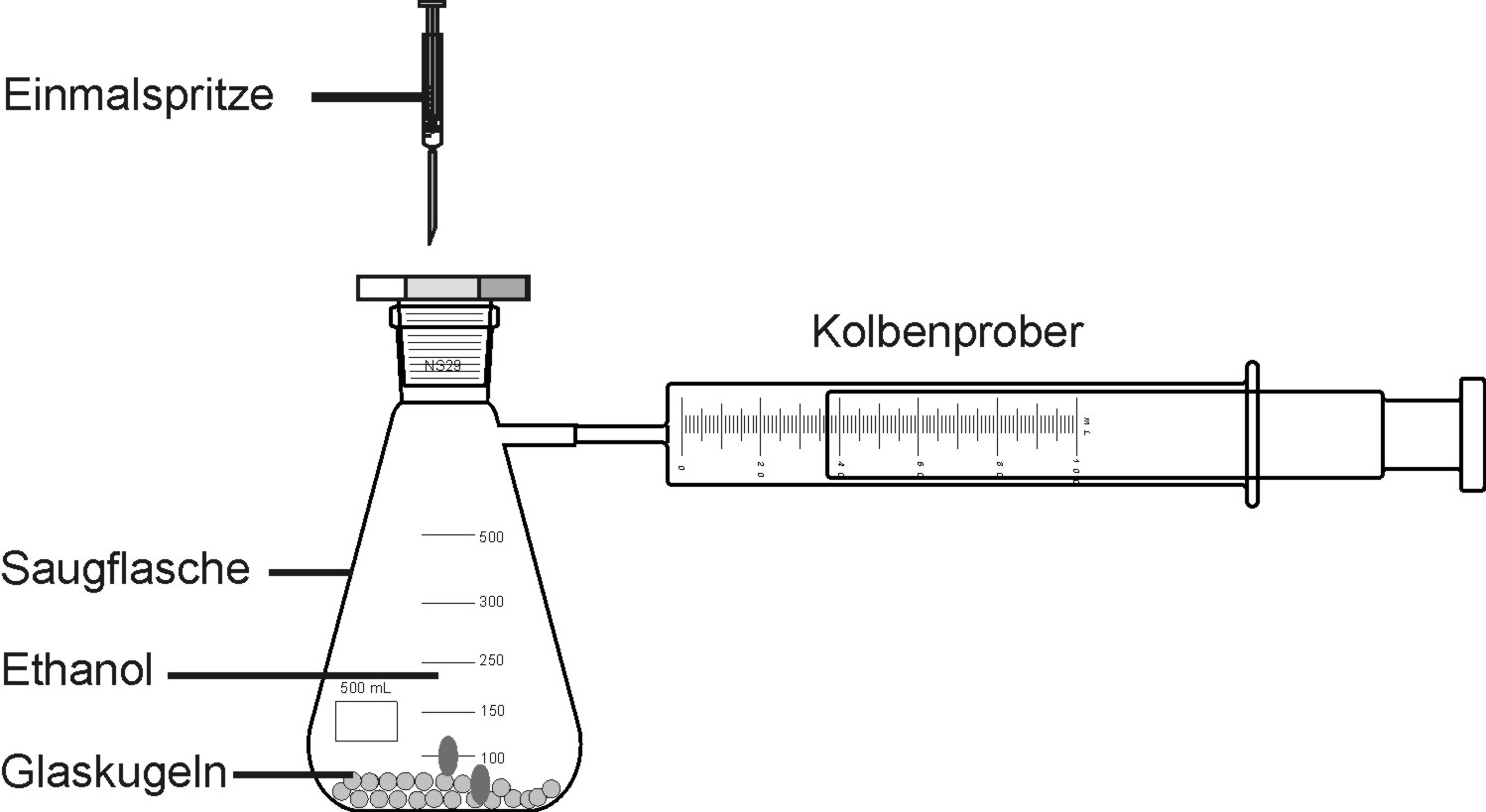
In den Erlenmeyerkolben werden 0,1 ml Ethanol eingespritzt. Auf der vergrößerten Oberfläche der Glasperlen wird das Ethanol leicht verdampft. Das entsprechende Gasvolumen kann am Kolbenprober abgelesen werden.
Auswertung:
0,1 ml Ethanol haben bei Standardbedingungen (SATP)* (25°C) ein Dampfvolumen von 43 ml.
0,1 ml Ethanol haben bei Normalbedinungen (0°C) ein Dampfvolumen von 37,8 ml.Eingesetzte Masse Ethanol: über Dichte:
ρ = Dichte
m = Masse
V = Volumen
Rechnung:
37,8 ml Ethanol (NB) haben die Masse 0,079 g: ρ = m/V = 0,079 g/37,8 ml = 0,0021 g/ml
Über das molare Gasvolumen bei Normalbedingung Vm (Gas) = 22,4 L kann man die Molmasse berechnen.
1 mol Ethanoldampf unter NB haben die Masse:
M(Ethanol) = (0,079 g * 22 400 ml)/37,8 ml = 46,8 g (Dreisatz)
{/sliders}
Literaturwert: M(Ethanol) = 46 g/mol.
_______________
* SATP-Bedingungen (Standard Ambient Temperature and Pressure)
-
5.1.3 Formelermittlung von Ethanol - Teil II
III. Quantitative Elementaranalyse
46g Ethanol ergeben bei der Verbrennung 88 g CO₂ und 54 g H₂O
- in 2 mol CO₂ sind 2 mol C (24g) enthalten
- in 3 mol H₂O sind 6 mol H (6g) enthalten
46 g Ethanol enthalten somit 2 mol C (24g) und 6 mol H (6g) und 1 mol (16g).
Atomzahlverhältnis im Ethanol: C : H : O = 2 : 6 : 1
Verhältnisformel: C₂H₆O₁
Molekülformel: C₂H₆O (Molekülmasse = 46u)IV. Ermittlung der Strukturformel von C₂H₆O
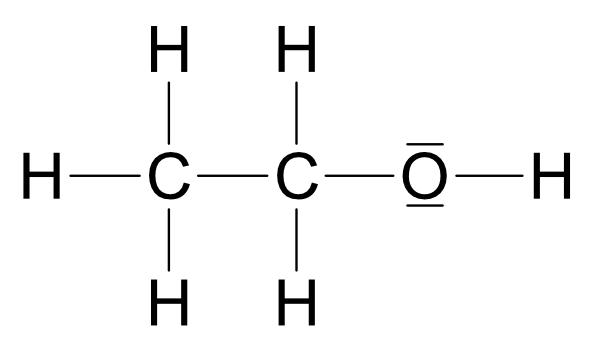
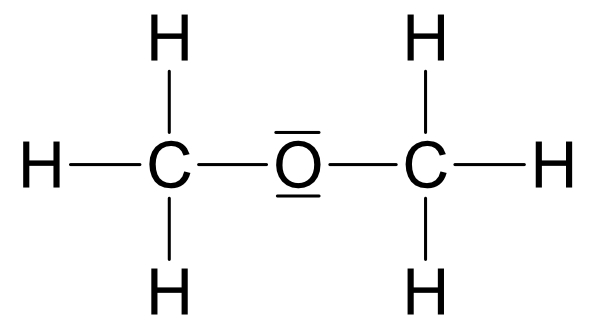
Zwei Möglichkeiten:
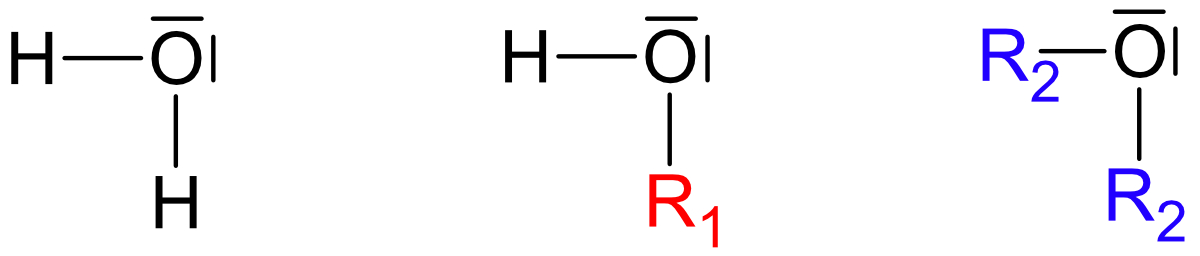
Wichtig: Ethanol und Dimethylether sind Derivate (Abkömmlinge) des Wassers.Beide Strukturen leiten sich vom Wasser ab, jedoch ist Struktur a wasserähnlicher.
R1 = - C₂H₅ (Ethylrest)
R2 = - CH₃ (Methylrest)
Siedepunkt: Struktur a +78°C und Struktur b -25°CUm herauszufinden, welche dieser Strukturen auf Ethanol zutrifft bitte nächste Seite anschauen.
-
5.1.4 Versuch Ethanol reagiert mit Alkalimetall
5.1.4 Versuch: Ethanol + Alkalimetall
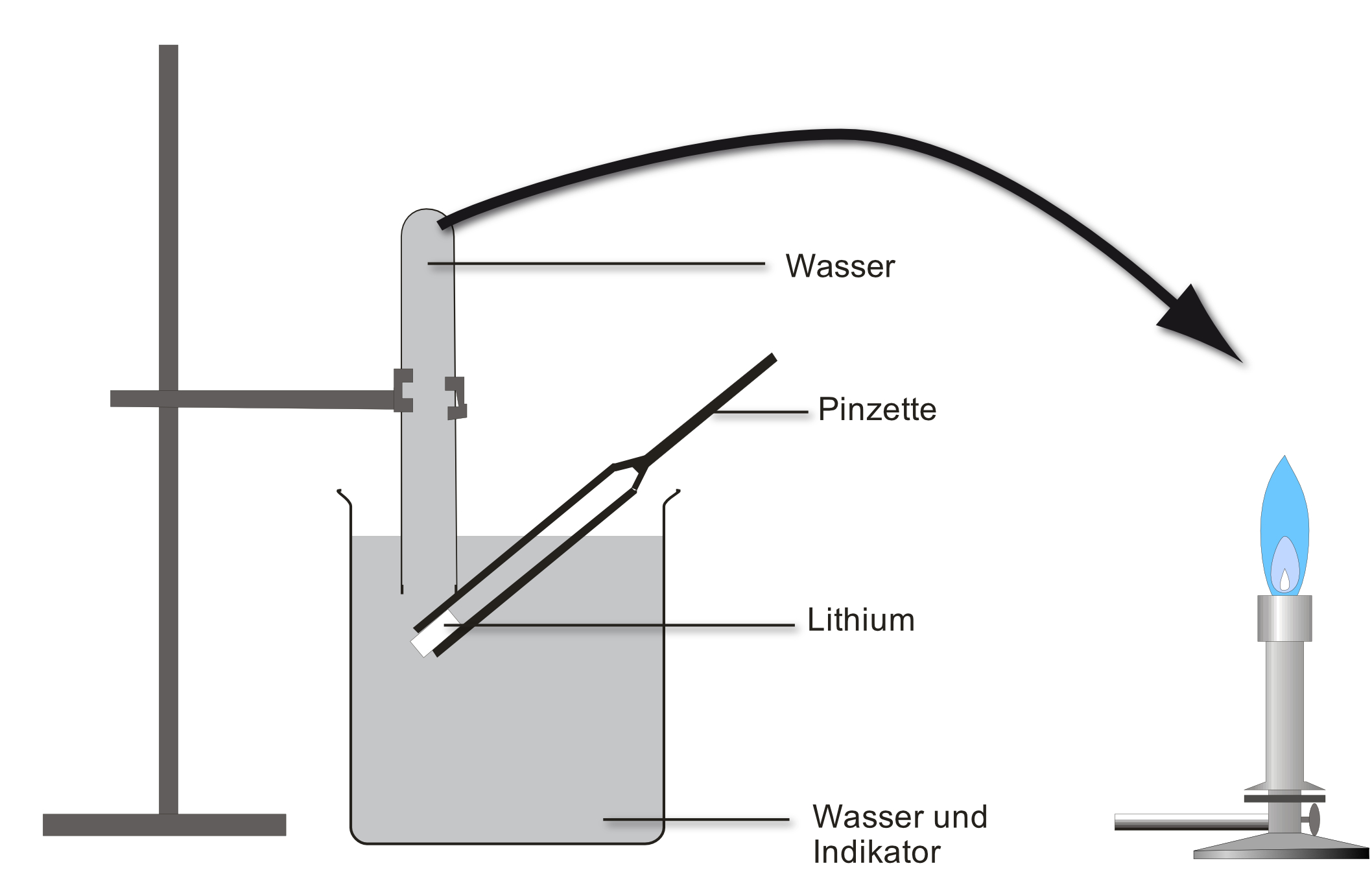
Versuch: Ein Stück Lithium ( SE ) wird auf Ethanol, Benzin und Wasser gegeben. Alternativ kann man die Experimente auch mit Natrium als Lehrerversuch durchführen. Die Reaktionsgleichungen sind mit dem Alkalimetall Natrium formuliert. Für Lithium gilt es analog.
Bei Wasser ist der Aufbau etwas komplizierter:
Beobachtung: Gasentwicklung; das entstehende Gas ist brennbar; Natrium „verschwindet“; die neu entstandene Lösung leitet den elektrischen Strom; dampft man die Lösung ein, entsteht ein weißer Feststoff.
Ergebnis:
Ethanol (Struktur a) reagiert mit Natrium unter Wasserstoffbildung. Struktur b (Dimethylether) würde so nicht reagieren, da sich kein Proton abspalten kann. Somit besitzt Ethanol die Strukturformel:
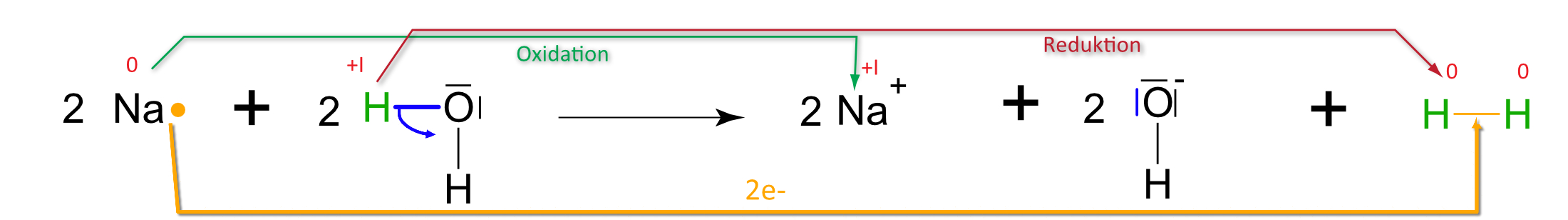
1. Natrium + Wassera) Teilchengleichung (mit Strukturformeln)
2 Na (s) + 2 H₂O (l) → 2 NaOH (aq) + H₂ (g) Natrium Wasser Natriumhydroxid Wasserstoff fest flüssig gelöst gasförmig 2. Natrium + Ethanol
Man kann Ethanol ja als Derivate (=Abkömmlinge) von Wasser betrachten. Wasser hat ein Sauerstoff-Atom und zwei Wasserstoff-Atome; Ethanol hat ein Sauerstoff-Atom, ein Wasserstoff-Atom und eine Ethyl-Gruppe. Beim Ethanol ist also ein Wasserstoff-Atom durch eine Ethylgruppe ersetzt. Wenn wir diese Alkylgruppe als "Rest" betrachten, dann zeigt sich die Verwandtschaft von Ethanol mit Wasser. Hat man also die Reaktionsgleichung von Wasser mit Natrium verstanden, dann müsste einem auch die Reaktionsgleichung von Ethanol (und anderen Alkoholen) leichtfallen. Versucht nun einmal, die Reaktion von Natrium mit Ethanol zu formulieren.
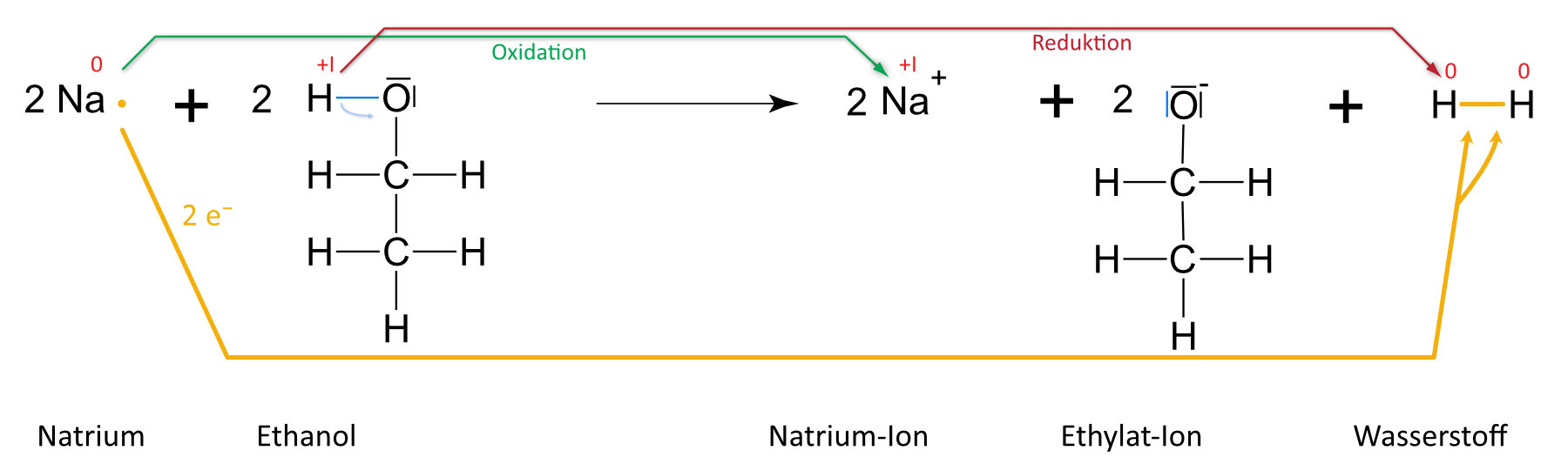
a) Teilchengleichung (mit Strukturformeln)
{slider title="Lösung" open="false" class="icon"}
{/sliders}
b) Reaktionsgleichung{slider title="Lösung" open="false" class="icon"}
2 Na (s) + 2 C₂H₅OH (l) 2 NaC₂H₅O (aq) + H₂ (g){/sliders}
Auswertung: Es ist keine „klassische“ Säure-Base-Reaktion nach Brönstedt. Grund: +I-Effekt (vgl. unten) der Methylgruppe (Protonierung ist erschwert). Es handelt sich hier um eine Redoxreaktion (Veränderung der Oxidationenszahlen). Formal geben zwei Moleküle Ethanol je ein Proton ab. Jedes Proton nimmt von einem Natrium- bzw. Lithiumatom ein Elektron auf; es bilden sich so zwei Wasserstoffatome, die sich zu einem Wasserstoffmolekül zusammenlagern. Analog, nur heftiger, verläuft die Reaktion mit Wasser.
Weitere Übungen:
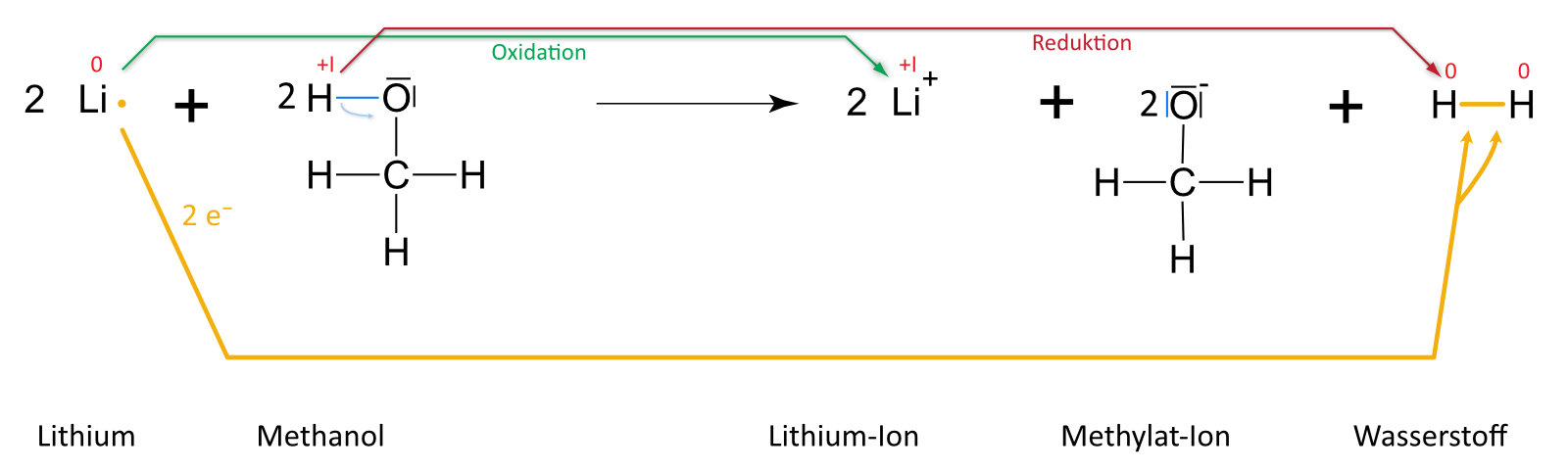
Lithium und Methanol
Formuliert auch dafür die Reaktionsgleichung (vgl. oben)
{slider title="Lösung" open="false" class="icon"}
{/sliders}
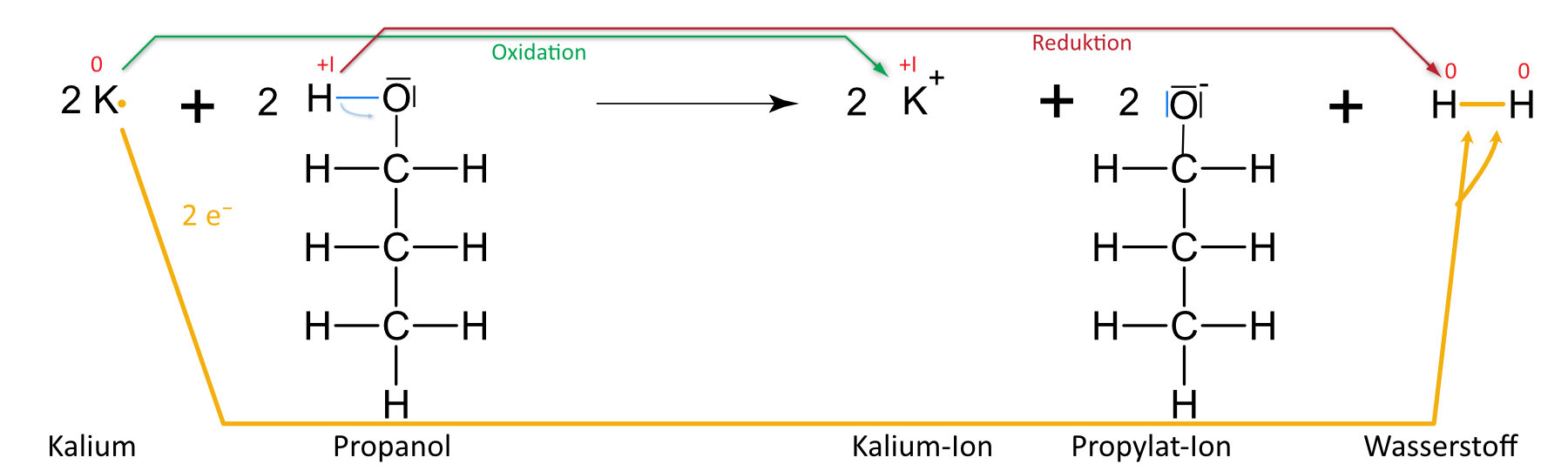
Kalium und Propanol
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
5.1.5 Induktiver Effekt
5.1.5 Induktiver Effekt (I-Effekt)
Ausschlaggebend: Elektronegativität (EN) der Substituenten (Atomgruppen, Atome die dranhängen). Dabei werden Elektronen über mehrere Bindungen angezogen oder „abgestoßen“.
Reichweite: 3 benachbarte Bindungen.
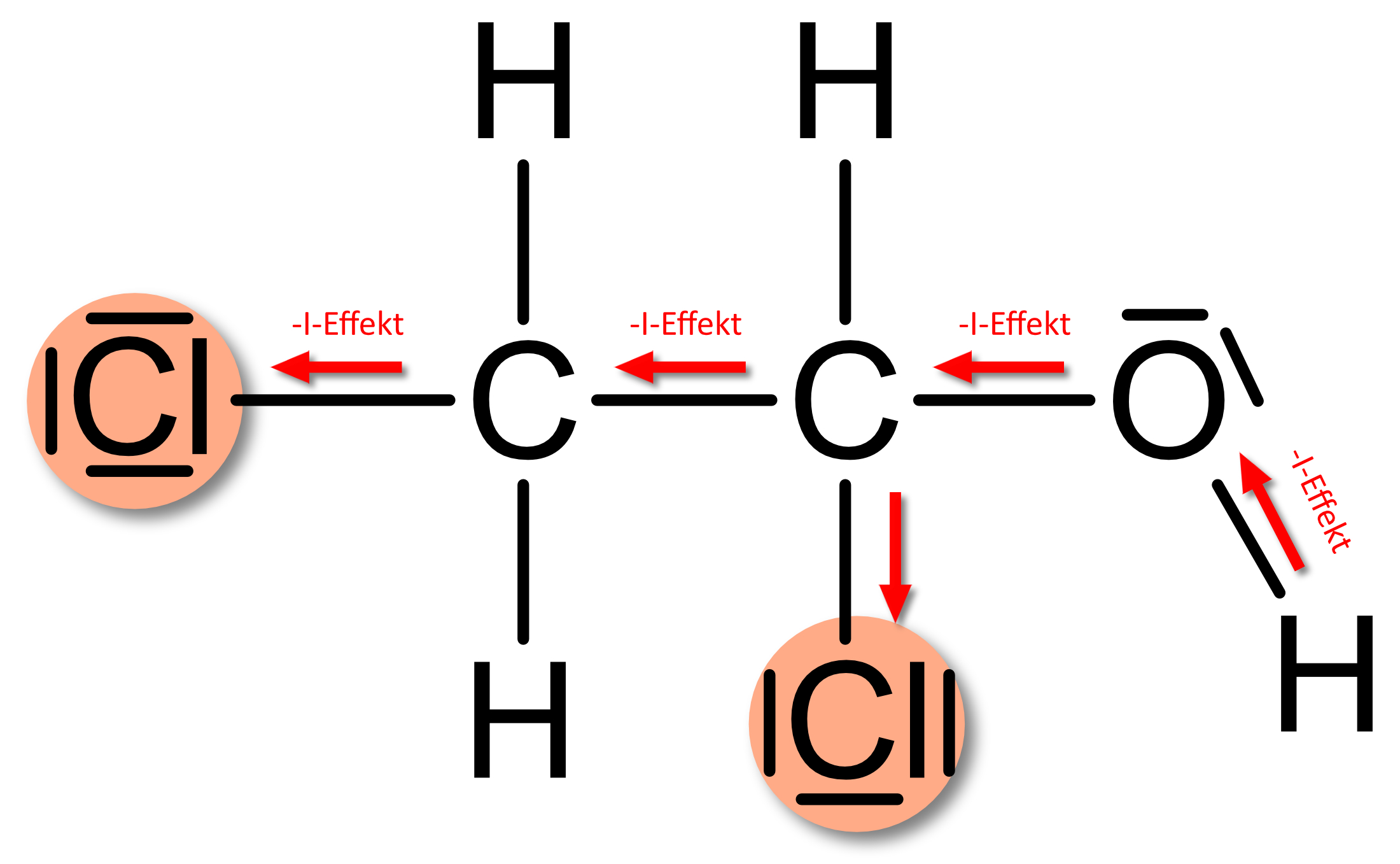
(-I)-Effekt (sprich: „minus I Effekt“; „negativer I Effekt“).• Substituenten (Atomgruppen) mit höherer Elektronegativität (Bsp.: Halogene, Sauerstoff-Verbindungen,...)• „Elektronenziehend“:
Ziehen Bindungselektronen zu sich
Auswirkung: z.B. Erleichterte Abspaltung eines Protons; Alkohol kann als Säure reagieren.
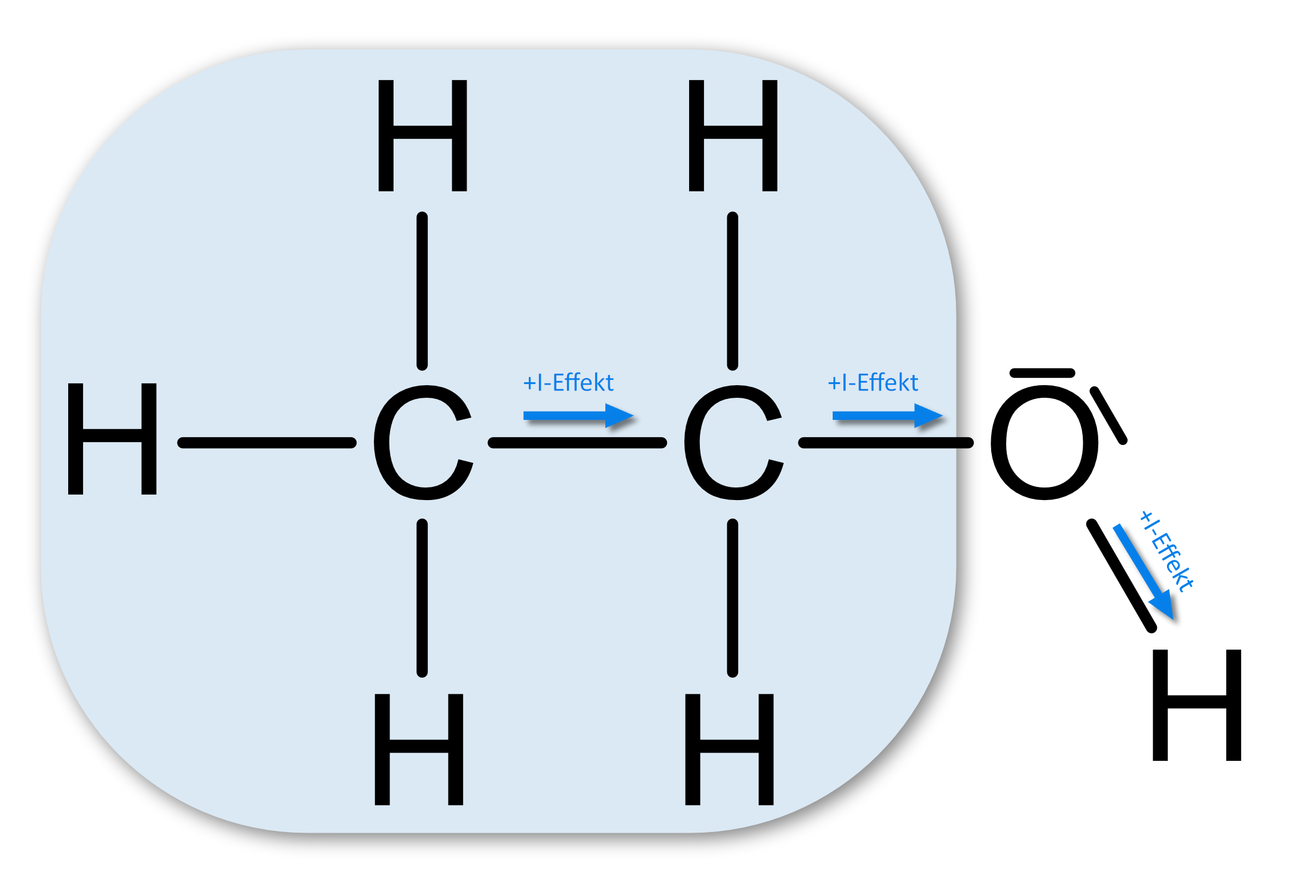
(+I)-Effekt (sprich: „plus I Effekt“; positiver I Effekt)Elektropositiveren Substituenten (Bsp.: Alkylgruppen). Je mehr bzw. je länger die Alkylgruppe, umso stärker ist der +-I-Effekt.
„Elektronenschiebend“:
Auswirkung: z.B. geringere Säurestärke
Keinen I-Effekt haben Wasserstoffatome.Auswirkung für das Experiment und Vergleich: Ethanol + Natrium und Wasser + Natrium
Bei diesem Experiment (siehe Seite zuvor) kommt es zu einer heftigeren Reaktion, wenn das Proton (vom Wasser oder Alkohol) leicht abgespalten wird. Je leichter es abgespalten wird, umso stärker ist ja auch seine Säure-Wirkung. Da Wasser keinen positiven induktiven Effekt hat (hat ja auch keine Alkylgruppe), reagiert es heftiger als Ethanol (positiver induktiver Effekt durch Alkylgruppe).
-
5.2 Homologe Reihe der Alkohole, Alkanole
5.2 Homologe Reihe der Alkohole, Alkanole
Vgl. AB
Vervollständige die Tabelle:
Name Strukturformel Summenformel Schmelztemp. Siedetemp. Aggregatzustand Löslichkeit in Wasser
Löslichkeit in Benzin Methanol - 96,9 °C 64,5 °C flüssig - 114,1 °C 78,5 °C flüssig - 126,5°C 97,4 °C flüssig - 89,5 °C 117,3 °C flüssig - 79,0 °C 137,3 °C flüssig ... ... ... ... ... ... Hexadecanol 50,0 °C 334,0 °C fest {slider title="Lösung" open="false" class="icon"}
{/sliders}
5.2.1 Alkohole bestehen aus zwei verschiedenen Gruppen:
Hydroxygruppe (früher Hydroxyl-Gruppe):
Sowohl vom positivierten Wasserstoff als auch vom negativierten Sauerstoff können Wasserstoffbrücken ausgehen (Hydrophiler Rest).
b) Alkylgruppe (bspw. "Methyl"):
Hier liegt kein positivierter Wasserstoff vor, es können sich keine Wasserstoffbrücken ausbilden (Hydrophober Rest).
5.2.2 Einige wichtige Alkohole
a) Methanol (Methylalkohol, „Holzgeist“): CH₃OH
Sdp.: + 65°C
Herstellung: Aus Methangas
Verwendung:- Zur Synthese in der chemischen Industrie
- Frostschutzmittel
Nachweis: Grüne Flamme von Trimethylborat LE
b) Ethanol (Ethylalkohol, „Weingeist“): C₂H₅OH
Sdp.: + 78°C
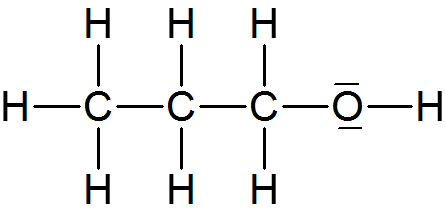
c) Propanol (Propylalkohol) C₃H₇OH
- 1-Propanol oder n-Propanol
Sdp.: 97°C
- 2-Propanol oder Isopropanol
Sdp.: +82°C
Verwendung: u.a. Lösungsmittel
d) Butanol (Butylalkohol);C₄H₉OH
Es gibt vier isomere Verbindungen:
AA: zeichnet alle 4 Isomere und beschriftet sie nach der Genfer Nomenklatur{slider title="Lösung" open="false" class="icon"}
I) 1-Butanol = Butan-1-ol: Sdp.: + 117°C
II) 2-Butanol: Sdp.: + 100°C
III) 2-Methyl-2-propanol = 2-Methyl-Propan-2-ol: + 83°C
IV) 2-Metyhl-1-propanol: + 108°C{/sliders}
5.2.3 Löslichkeit von primären und unverzweigten Alkoholen
Löslichkeit von... in Wasser in Benzin Methanol gut wenig Ethanol gut gut 1-Propanol gut gut 1-Butanol wenig gut 1-Pentanol wenig gut Versuchsskizze: Methanol + Benzin
Merke: Je länger das Alkoholmolekül, desto ähnlicher den Alkanen (unähnlicher dem Wasser).
Allgemein gilt: „Ähnliches löst sich in Ähnlichem“
Niedere (kurzkettigere) Alkohole können Solvathüllen bilden deshalb Salze lösen (jedoch schlechter als Wasser!). Es gibt sogar feste Salze mit „Kristallalkohol“. (analog: Salze mit Hydratwasser).
-
5.2.4 Primäre, sekundäre und tertiäre Alkohole
5.2.4 Primäre, sekundäre und tertiäre Alkohole
a) Bei primären Alkoholen ist das C-Atom, das die OH -Gruppe trägt, an höchstens ein weiters C-Atom gebunden.
Bsp.: Ethanolb) Bei sekundären Alkoholen ist das C-Atom, das die OH -Gruppe trägt, an zwei weitere C-Atome gebunden.
Skizziert zunächst selbständig eine Strukturformel, für welches die Definition gilt:
{slider title="Lösung" open="false" class="icon"}
Bsp.: 2-Propanol
Die "zwei weiteren C-Atome" sind grün markiert.
{/sliders}
c) Bei tertiären Alkoholen... (vervollständigt die Definition und zeichnet ein mögliches Molekül):
{slider title="Lösung" open="false" class="icon"}
...ist das OH-Gruppe tragende C-Atom an 3 weitere C-Atome gebunden.
Bsp.: 2-Methyl-2-propanol:{/sliders}
5.2.5 Allgemeine Molekülformel der Alkohole (Alkanole)
CnH2n+1OH
Alle Alkohole enthalten die Hydroxygruppe (Hydroxylgruppe) als funktionelle Gruppe. -
5.3 Chemische Reaktionen von Alkohol
5.3 Chemische Reaktionen von Alkohol, Alkanol (am Beispiel von Ethanol)
5.3.1 Bindungsverhältnisse
5.3.2 Ethanol und Natrium (Redoxreaktion)
Ein Thema, welches schon zuvor angesprochen wurde.
5.3.3 Verbrennung von Ethanol
Übung: Formuliere eine Reaktionsgleichung für die vollständige Verbrennung von Ethanol. Bestimme hierfür auch die Atome, die oxidiert und die reduziert wurden und begründe Deine Wahl.
{slider title="Lösung" open="false" class="icon"}
Oxidation = Erhöhung der Oxidationszahlen („e- Abgabe“) ⇨ C
Reduktion = Erniedrigung der Oxidationszahlen („e- Aufnahme“) ⇨O (nur der Luftsauerstoff){/sliders}
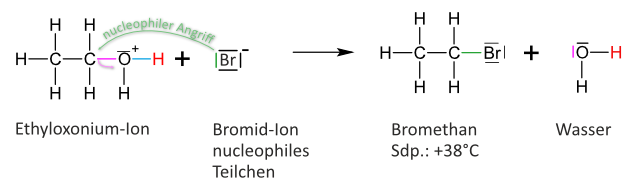
5.3.4 Reaktion von Ethanol mit Bromwasserstoffsäure
Im Mikroglasbaukasten werden 1ml Ethanol mit 4 ml HBr erhitzt. Das entstehende Produkt wird in Wasser eingeleitet. Das neue Produkt (Bromethan) besitzt eine größere Dichte als Wasser.
Ablauf der Reaktion:
1. Schritt: Protonierung
⇒ Säure-Base-Reaktion2. Schritt: Nucleophile Substitution
Es handelt sich also um eine nucleophile Substitution, SN-Reaktion.
Substitution an Alkoholen laufen meist erst nach Protonierung ab! Ein Hydroxidion (OH⁻ ) ist stärker nucleophil und viel schwerer abzuspalten als ein Wassermolekül (schwach nucleophil).