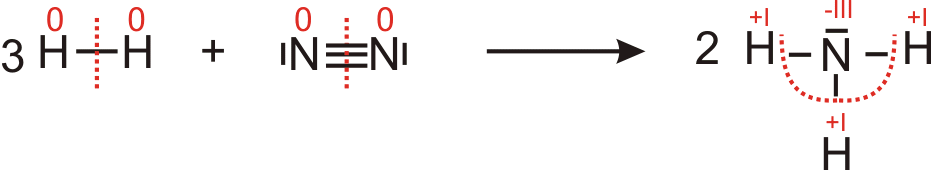Elektronegativität
-
3 Redoxreaktionen mit Molekülen - Oxidationszahlen
3 Redoxreaktionen mit Molekülen
Bei der Verbrennung von Stoffen bilden sich Oxide, ohne dass es zur Bildung von Ionen kommt. Beispiele dafür sind die Verbrennung von Wasserstoff, Kohlenstoff, Schwefel und Phosphor.
Um diese Reaktion als Redoxreaktion erfassen zu können, hat man als Hilfsgröße die Oxidationszahl eingeführt.
3.1 Oxidationszahl
Def.: Die Oxidationszahl gibt an, welche Ladung ein Atom in einem Molekül oder in einem anderen Teilchen hätte, wenn alle am Aufbau des Teilchens beteiligten Atome in Form von Ionen vorlägen.
Die sich für die Atome in der Verbindung ergebenden formalen Ladungszahlen nennt man Oxidationszahlen. Zur Unterscheidung von Ionenladungen werden sie als römische Zahlen an die Elementsymbole geschrieben.
Vorgehensweise: Vgl. dazu die zwei Beispiele 3.2 und 3.3 um die Schritte nachvollziehen zu können.
1. Schritt: Strukturformel erstellen.
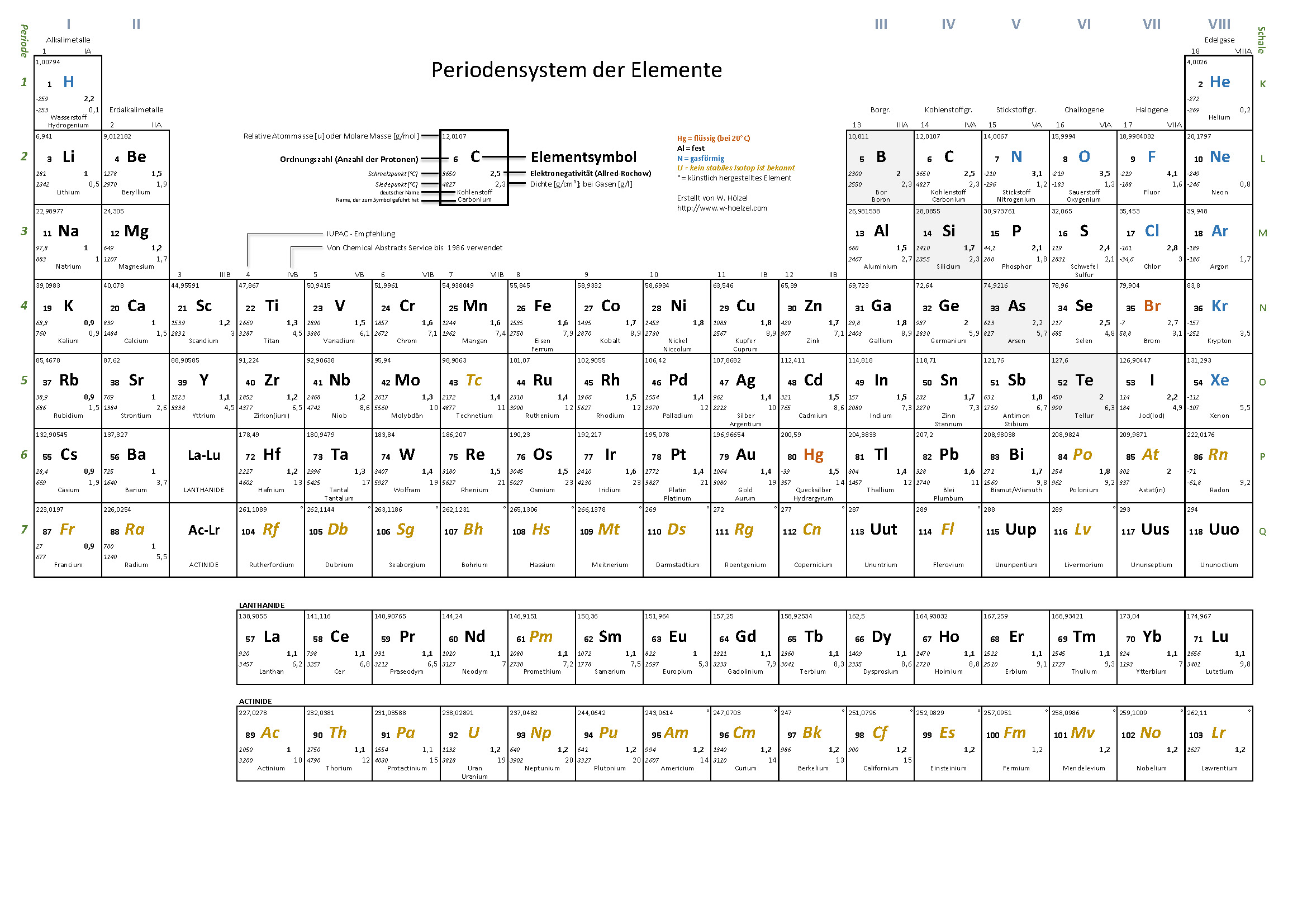
2. Schritt: Ermittlung der Elektronegativität aller Elemente (siehe PSE) :
3. Schritt: Bindungselektronen werden formal dem elektronegativeren Bindungspartner zugeteilt. Besitzen die Bindungspartner die gleiche Elektronegativität erhalten sie je die Hälfte der Bindungselektronen.Faustregel: (Hinweis: Wann immer eindeutige Strukturformeln möglich sind, würde ich keine Faustregeln nutzen)
- Fluor immer: –I
- Wasserstoff: +I
- Sauerstoff: -II
- Halogene: -I (sofern nicht mit Sauerstoff oder einem elektronegativeren Halogen verbunden sind)
4. Schritt: Man bestimmt die Hauptgruppennummer des Elements und zählt dann die Elektronen, welche das Element jetzt "formal" hätte (vgl. 3. Schritt). Dann berechnet man entsprechend folgender Formel:
Oxidationszahl = Hauptgruppennummer des Elements – Elektronenanzahl im Molekül
Bsp. Sauerstoff im Wassermolekül: Oxidationszahl(O) = steht in der 6. Hauptgruppe = VI - 8 = -2 (bzw. - II)
Bsp. Wasserstoff im Wassermolekül: Oxidationszahl(H) = I - 0 = +1
5. Schritt: Kontrolle: Summe der Oxidationszahlen muss 0 sein (bei elektr. Neutralen Molekülen).
Mit Hilfe der Oxidationszahl lassen sich die Begriffe Oxidation und Reduktion neu fassen:Oxidation: Elektronenabgabe) bedeutet eine Erhöhung der Oxidationszahl.
Reduktion: (Elektronenaufnahme) bedeutet eine Erniedrigung der Oxidationszahl.
Redoxreaktionen: sind Vorgänge bei denen sich die Oxidationszahlen der beteiligten Atomarten ändern.3.2 Vollständige Verbrennung von Kohlenstoff
Kohlenstoff Sauerstoff Kohlenstoff(IV)-oxid
Atom Molekül Molekül

→ Kohlenstoff wird oxidiert, Sauerstoff wird reduziert.3.3 Reaktion von Wasserstoff mit Sauerstoff
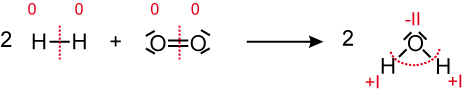
Wasserstoff Sauerstoff Wasser
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wird oxidiert
Oxidationszahlen von Sauerstoff wird negativer → Sauerstoff wird reduziert3.5 Reaktion von Wasserstoff mit Stickstoff zu Ammoniak (Ammoniaksynthese)
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
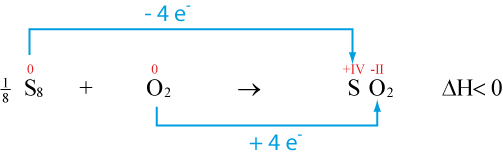
Oxidationszahlen von Stickestoff wurde negativer → Stickstoff wurde reduziert3.6 Reaktion von Schwefel mit Sauerstoff zu Schwefeldioxid
Man muss nicht immer die Lewis-Formeln (Strukturformeln) zeichnen. Manchmal genügt es, nach den Faustregeln zu arbeiten.
Oxidationszahlen von Schwefel wird positiver → Schwefel wurde oxidiert
Oxidationszahlen von Sauerstoff wurde negativer → Sauerstoff wurde reduziert3.7 Synthese von Chlorwasserstoff aus den Elementen
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Chor wurde negativer → Chlor wurde reduziert3.8 Synthese von Schwefelwasserstoff aus den Elementen
Oxidationszahlen von Wasserstoff wird positiver → Wasserstoff wurde oxidiert
Oxidationszahlen von Schwefel wurde negativer → Schwefel wurde reduziert -
4.4 Polare und unpolare Atombindung
4.4 Polare und unpolare Atombindung
Auch dafür gibt es eine mehr interaktive Seite:
{slider title="Link zur interaktiven Übungsseite mit Bildern" open="false" class="icon"}
{/sliders}
4.4.1 Unpolare Atombindung
Bei der unpolarenAtombindung werden die Bindungselektronenvon beiden Atomen gleich oder nahezu gleich angezogen. Bsp.: O₂, Cl₂, etc.
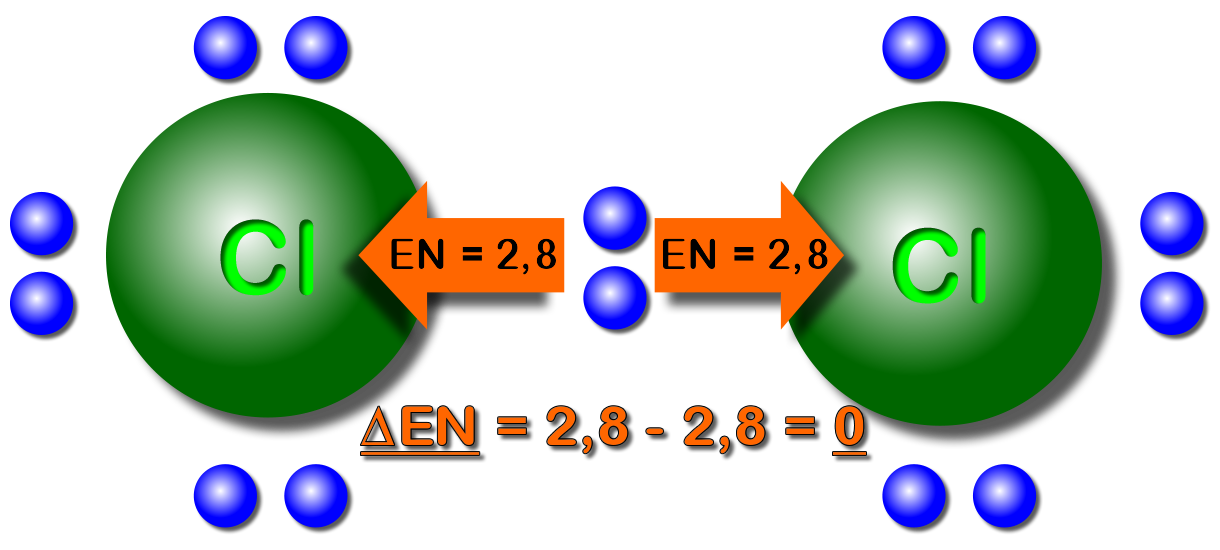
Am Beispiel vom Chlor-Molekül etwas erklärt.
Da beide Chlor-Atome die gleiche Elektronegativität ("Geilheit nach Elektronen") haben, ziehen sie gleich stark. Die Elektronen sind somit in der "Mitte" der beiden Atomkerne. Die Elektronegativitätdifferenz ist 0 ("Null").
Veranschaulichen kann man die Elektronenverteilung mit Hilfe der Federn aus der Physik. Wenn eine Kugel mit gleichstarken Federn befestigt wurde, so ist die Kugel genau in der Mitte. Auch wenn ich die Kugel z.B. nach rechts verschiebe, wird sie sich wieder in die Mitte einpendeln.
Wichtige Faustregel: Bei einer Elektronegativitätsdifferenz (ΔEN) von 0 bis etwa 0,4 spricht man von einer unpolarenAtombindung. 4.4.2 Polare Atombindung
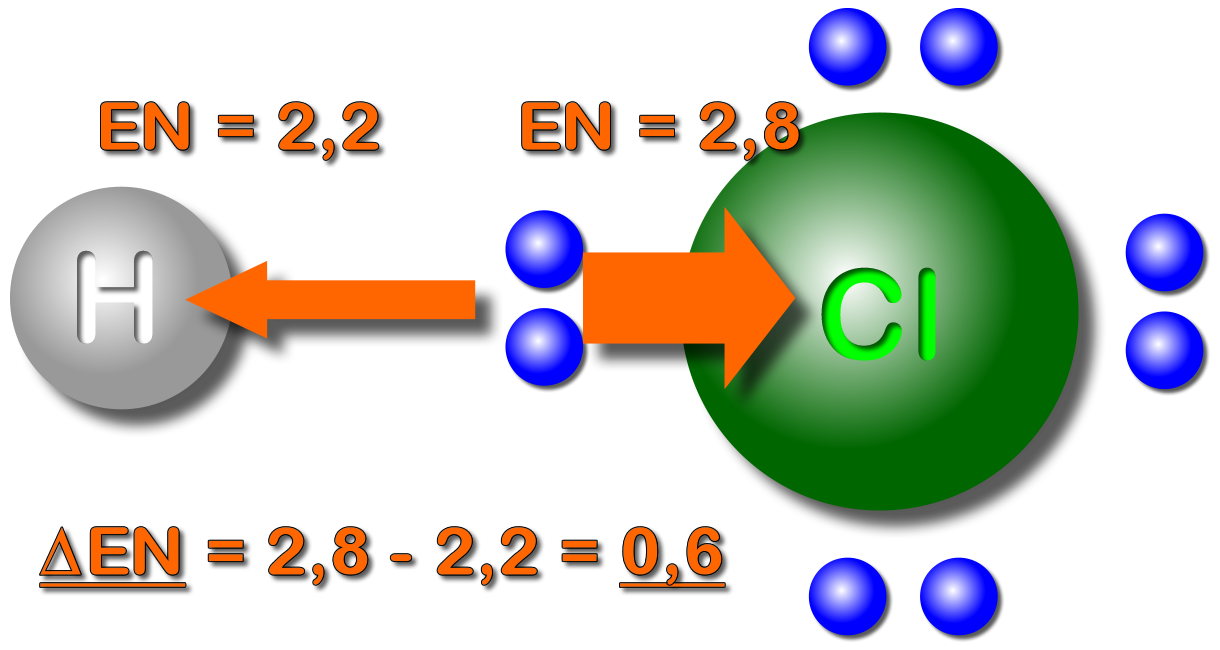
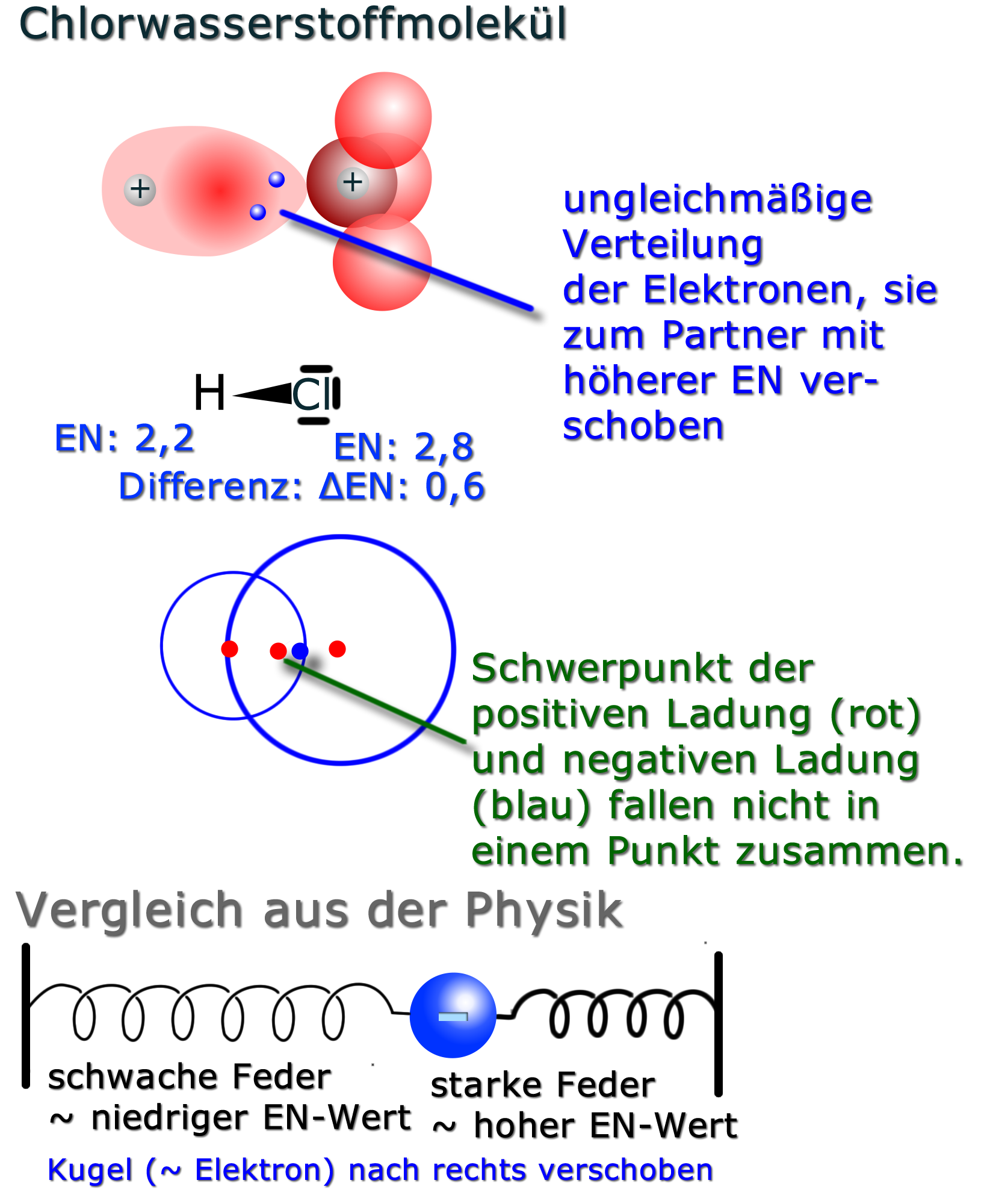
Bei der polarenBindung werden die Bindungselektronenvon einem Atom stärker angezogen als von dem anderen. Dadurch ist die Elektronenwolke zum Atom mit der höheren EN verschoben.
Durch die asymmetrische Verteilung der Elektronen kommt es zu Teilladungen.
Man kennzeichnet die Ladungsverschiebung mit den Symbolen für Teilladungen δ+ und δ- („delta plus bzw. delta minus“) und/oder mit der Keilschreibweise: Hierbei macht man die Seite der Atombindung "dicker", die "mehr" Elektronen hat (bzw. wohin die Elektronen verschoben sind).Vom gleichen Molekül hier noch ein paar weitere Erklärung mit Hilfe unterschiedlicher Abbildungen:
Auch hier kann der Vergleich aus der Physik bei der Vorstellung helfen. Hierbei ist die Kugel in Richtung der stärkeren Feder verschoben.
Wichtige Faustregel: Bei einer Elektronegativitätsdifferenz (ΔEN) von etwa 0,4 bis etwa 1,8 spricht man von einer polarenAtombindung. -
Periodensystem der Elemente - PSE
Ich habe für meine Schüler Periodensysteme erstellt, die jederzeit ausgedruckt werden können. Das Ziel: je nach Aufgabenstellung nur die wesentlichen Informationen. Die Werte stammen aus verschiedenen Quellen (www.wikipedia.de, www.internetchemie.info, Mortimer „Chemie", Holleman-Wiberg „Lehrbuch der anorganischen Chemie").
Falls gravierende Fehler vorhanden sind, würde ich mich über eine Nachricht freuen. Diese Periodensysteme können heruntergeladen und ausgedruckt werden.
Kurze Einführung in das Periodensystem der Elemente
Eine kurze Einführung in das PSE mit einfachen Übungen findest du auf meiner Basischemie-Seite. Allerdings ist das empfohlene PSE nicht mehr online (weshalb ich selber welche erstellte; vgl. unten).
Periodensysteme
1. Einfaches PSE für die Schule
Beschränkt sich auf die wesentlichen Informationen. Auch die Halbmetalle sind sehr einfach wiedergegeben.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vereinfacht; vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- Aggregatzustand bei 20 °C

3. PSE – Nur Hauptgruppenelemente
Für Edelgasregel, Atombindungen und erste Salze — ohne Nebengruppen.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- KEINE Nebengruppen, Lanthanide, Actinide
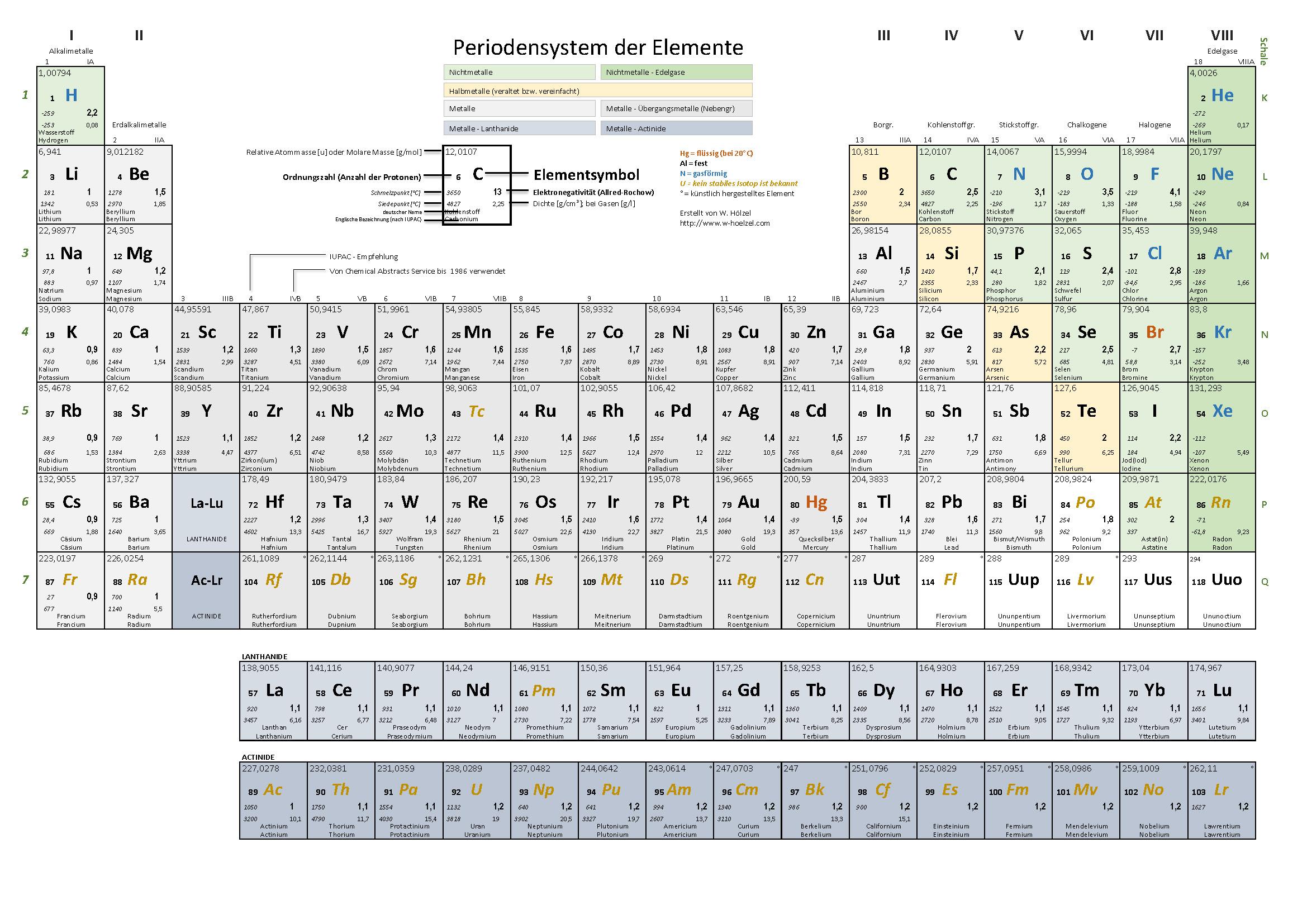
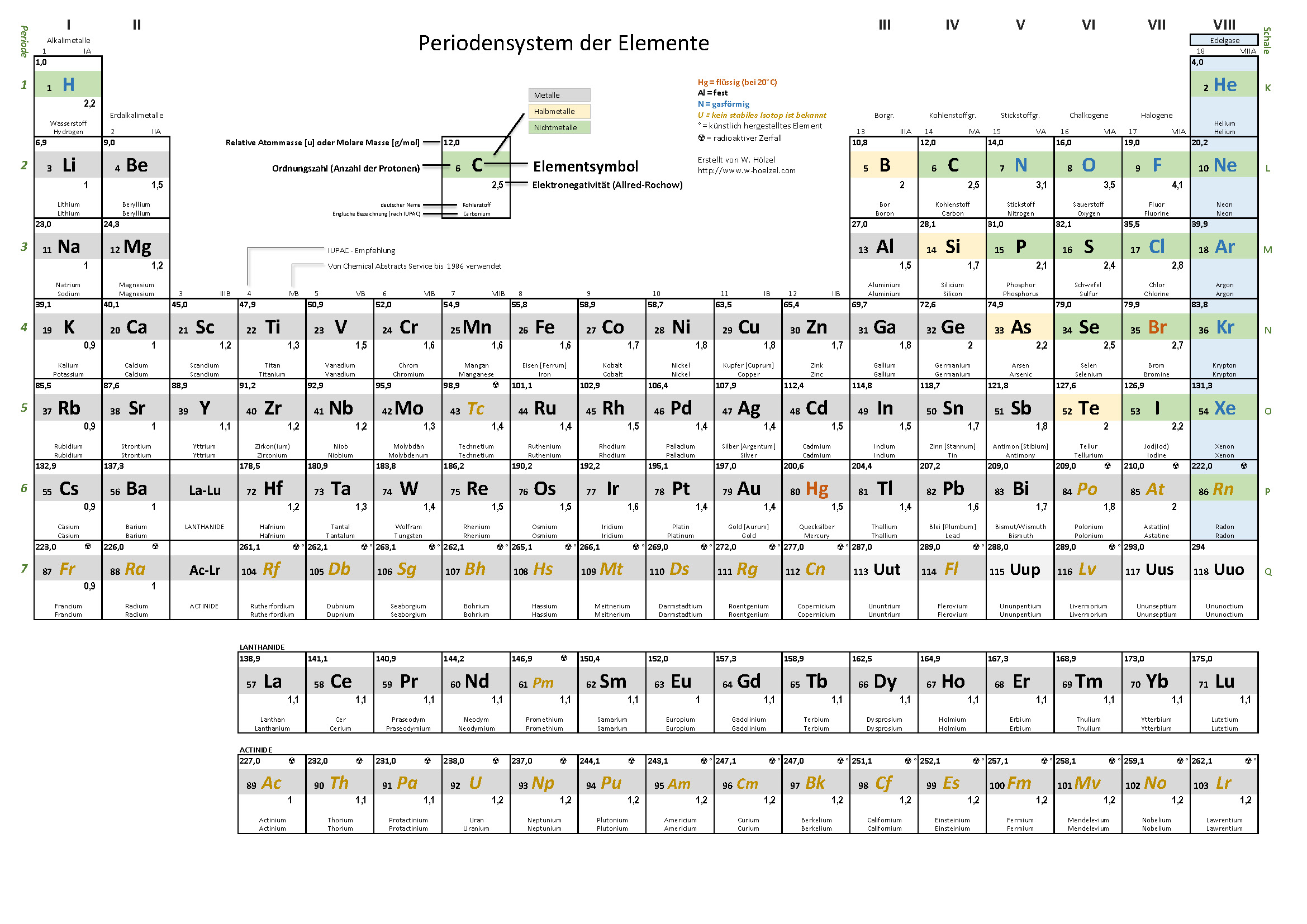
6. PSE – Einteilung Metalle / Nichtmetalle
Farbige Einteilung der Metalle, Halbmetalle, Nichtmetalle und Edelgase.
- Elektronegativität
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Halbmetalle (vgl. Wikipedia)
- Metalle · Nichtmetalle · Edelgase
- Aggregatzustand · Dichte · Schmelz- und Siedetemperatur
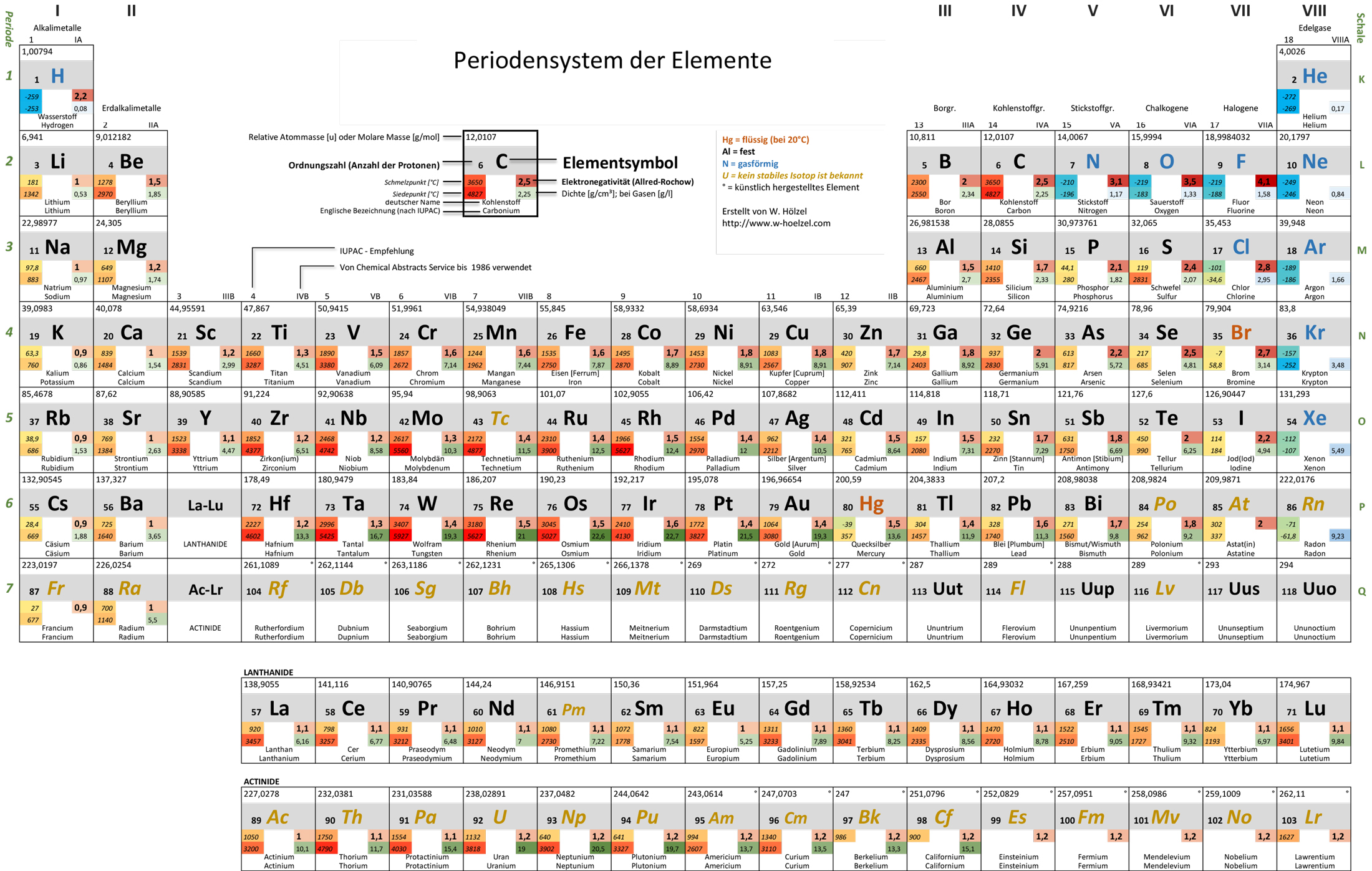
10. PSE – Farbkodierung für Eigenschaften
Visualisiert Schmelztemperatur, Siedetemperatur, Dichte und Elektronegativität mittels Farbkodierung.
- Elektronegativität [farbig]
- Namen (deutsch und englisch)
- Ordnungsnummer · Masse · Symbol
- Aggregatzustand · Dichte [farbig]
- Schmelztemperatur [farbig] · Siedetemperatur [farbig]
Einige Beispiele weiterer Periodensysteme im Internet
- Zentrale Übersicht: https://de.wikipedia.org/wiki/Periodensystem
- Hervorragende Datensammlung: www.internetchemie.info
- Interaktives PSE mit Elektronenverteilung und Wikipedia-Links: www.ptable.com
- Interaktives PSE mit PSE-Ansichten: www.uniterra.de