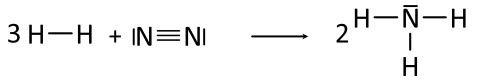Atombindung
-
4 Atombindung = Elektronenpaarbindung
4 Atombindung = Elektronenpaarbindung
{slider title="Link zur interaktiven Übungsseite mit Bildern" open="false" class="icon"}
Hier empfehle ich auf jeden Fall die Übungsseite!
{/sliders}
Beispiel 1: Bildung eines Wasserstoffmolekül (H₂)
Nähern sich zwei Wasserstoffatome (H•), so können sich die beiden „Kugelwolken“ (Orbitale) in einem gewissen Ausmaß durchdringen („überlappen“). Es bildet sich eine neue Molekülorbital, die beide Atomkerneumschließt.

Zwischen den beiden Kernenkommt es zu einer Verdichtung der negativenLadung, zu der beide Elektronen gleichviel beitragen und die zur Anziehung zwischen den beiden positivgeladenen Kernen führt. Die beiden Elektronen bezeichnet man als bindendes Elektronenpaar. Beide Atome nutzen das Elektronenpaar gemeinsam.
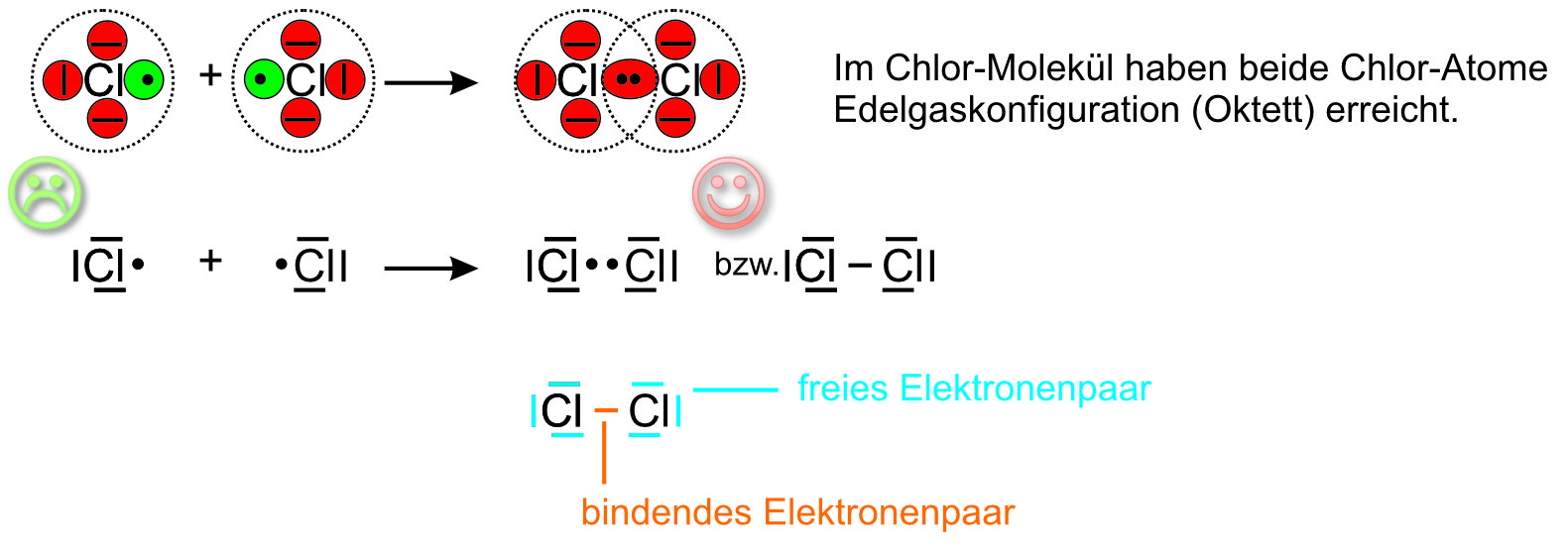
Beispiel 2: Bildung eines Chlor-Moleküls, Cl₂-Molekül
Versucht nun einmal selbständig die Abbildungen vom Wasserstoff oben auf das Beispiel Chlor zu übertragen. Kommt ihr nicht weiter oder seid ihr fertig, macht die Lösung auf.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
Bindigkeit: Zahl der von einem Atom gebildeten Atombindung.
Im Chlormolekül ist Chlor einbindig; beide Chlor-Atome gelangen durch das gemeinsame (bindende) Elektronenpaar in den Besitz von 8 Außenelektronen (Oktett, Edelgaskonfiguration).Beispiel 3: Bildung eines Stickstoffmoleküls, N₂-Moleküls
Jetzt solltet ihr einmal die Bildung eines Stickstoffmoleküls zeichnen (einmal noch nach den Kugelwolkenmodell und einmal in Lewis-Formel):
{slider title="Lösung" open="false" class="icon"}
{/sliders}
-
4.1.1 Die Elektronenpaar-Bindung und die HNO-Regel
4.1.1 Die Elektronenpaar-Bindung und die HNO-Regel
Die HNO-Regel hat leider ein paar Konsequenzen, die die Sache verkomplizieren. Wir werden immer wieder die gleichen chemischen Reaktionen anschauen, aber sie unterschiedliche Aufschreiben; wundert Euch also nicht, dass Euch manches bekantn vorkommt bzw. dass wir die Reaktionsgleichungen etwas unterschiedlich. Aber ihr wisst auch, dass man durch Wiederholung am besten lernt.
In diesem Kapitel geht es darum, zu verstehen, warum es eine einfache und eine etwas kompliziertere Reaktionsgleichung gibt, weil wir die HNO-Regel anwenden müssen.
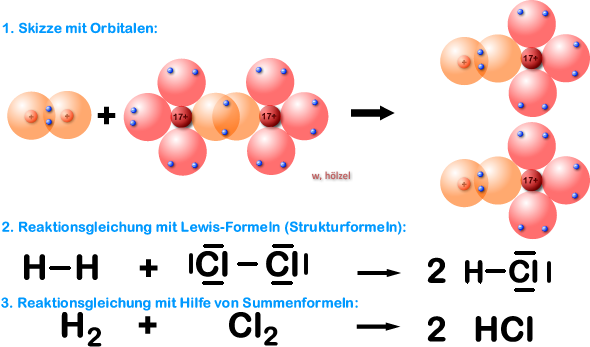
Beispiel 4a: Bildung eines Chlorwasserstoff-Moleküls, HCl-Molekül - ohne HNO-Regel.
Jetzt solltet ihr ein Molekül aus zwei unterschiedlichen Elementen herstellen (Element Wasserstoff und Element Chlor). Wir haben also ein Wasserstoff-Atom, welches mit einem Chlor-Atom reagieren soll. Das Ergebnis ist Chlorwasserstoff.
Im Chlorwasserstoff-Molekül liegt eine Einfachbindung vor; somit ist Chlor und Wasserstoff im Chlorwasserstoff-Molekül einbindig.
Im Chlorwasserstoff-Molekül erlangt das Chlor-Atom durch das gemeinsame (bindende) Elektronen-paar 8 Valenzelektronen (Edelgaskonfiguration, Oktett; Argon-Atom) und das Wasserstoff-Atom durch das binden-de Elektronenpaar 2 Außenelektronen (ebenfalls Edelgaskonfiguration; Helium-Atom) (siehe gestrichelte Kreise oben).
Bei den Ausgangsstoffen wird die Edelgas-Regel aber nicht erfüllt.
Beispiel 4b: Bildung eines Chlorwasserstoff-Moleküls, HCl-Molekül - mit HNO-Regel.
Frage: Für welche Ausgangsstoffe müssen wir die HNO-Regel anwenden?
{slider title="Lösung" open="false" class="icon"}
Für beide. H-Atom kommt in "HNO" vor und Cl-Atom ist ein "Hal"ogen.
{/sliders}
Aufgabe: Formuliere die Bildung des Moleküls von Chlorwasser mit Berücksichtigung der HNO-Regel
{slider title="Lösung" open="false" class="icon"}
Wichtig bei Reaktionsgleichungen ist natürlich, dass man immer gleich viel von jeder Atomsorte hat. Dabei darf man die Anzahl frei wählen.
Zur Veranschaulichung auch nochmal eine Abbildung mit den Kugelwolken. Die Summenformel zum Schluss werden im nächsten Kapitel genauer erklärt.
{/sliders}
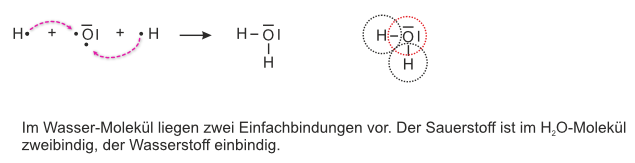
Beispiel 5a: Bildung eines Wassers-Moleküls, H₂O-Molekül - ohne HNO-Regel.
Wasser besteht aus Wasserstoff und Sauerstoff.
Aufgabe: Schreibt zunächst für die Bildung von Wasser aus seinen Elementen Wasserstoff und Sauerstoff die Reaktionsgleichung ohne Berücksichtigung der HNO-Regel:
{slider title="Lösung" open="false" class="icon"}
{/sliders}
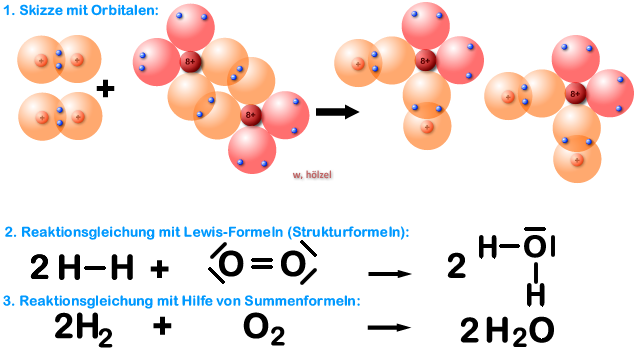
Beispiel 5b: Bildung eines Wassers-Moleküls, H₂O-Molekül - mit HNO-Regel.
Aufgabe: Schreibt jetzt die Reaktionsgleichung mit der HNO-Regel. Hinweis: Die Lösung habe ich nochmals zusätzlich mit Kugelwolkenmodell gemacht.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
Beispiel 6a: Bildung eines Ammoniak-Moleküls, NH₃-Molekül - ohne HNO-Regel.
Aufgabe: Zum Schluss der solltet ihr einmal Ammoniak aus seinen beiden Elementen Wasserstoff und Stickstoff herstellen - ohne HNO-Regel. Kleiner Tipp: Euch ist bestimmt schon aufgefallen, dass wann immer ein Einzelelektron (= Punkt in der Lewis-Formel) vorliegt, sich dieses bei den Atombindungen einen Partner sucht und versucht sich zu verbinden. Kontrolliert zum Schluss nochmals, ob die Edelgas-Regel erfüllt ist.
{slider title="Lösung" open="false" class="icon"}
{/sliders}
Beispiel 6b: Bildung eines Ammoniak-Moleküls, NH₃-Molekül - mit HNO-Regel.
Aufgabe: Formuliert die Reaktionsgleichung für die Bildung von Ammoniak in Lewis-Formeln mit Berücksichtigung der HNO-Regel:
{slider title="Lösung" open="false" class="icon"}
Jedes mal zum Ausgleichen die ganzen Strukturformeln hinzuschreiben ist sehr zeitaufwendig (und eigentlich auch unnötig). Man schreibt viel einfacher die Ziffer davor.
{/sliders}
Zusammenfassung:
Eine Atombindung entsteht durch „Überlappung“ zweier (oder mehrerer) einfach besetzter Atomorbitale. Dies ist ein exothermerVorgang. Die Element-Atome erreichen im Molekül durch gemeinsamen Elektronenbesitz Edelgaskonfiguration. -
4.3 Reaktionsgleichungen in Lewis-Schreibweise und Summenformeln
4.3 Reaktionsgleichungen in Lewis-Schreibweise und Summenformeln
Jetzt kommt nichts neues mehr sondern nur zusammenfassend die vorherigen Themen als Übungen kurz und knapp verbunden. Ihr müsst für alle Aufgaben die Edelgas-Regel und die HNO-Regel anwenden.
1. Übung: Formuliert für die Synthese von Wasser aus seinen Elementen die Reaktionsgleichung in (a) Lewis-Schreibweise und (b) mit Hilfe von Summenformeln.
{slider title="Lösung" open="false" class="icon"}
2 H₂ + O₂ → 2 H₂O
{/sliders}
2. Übung: Formuliert für die Synthese von Ammoniak aus seinen Elementen die Reaktionsgleichung in (a) Lewis-Schreibweise und (b) mit Hilfe von Summenformeln.
{slider title="Lösung" open="false" class="icon"}
3 H₂ + N₂ → 2 NH₃
{/sliders}
3. Übung: Formuliert für die Synthese von Chlorwasserstoff aus seinen Elementen die Reaktionsgleichung in (a) Lewis-Schreibweise und (b) mit Hilfe von Summenformeln.
{slider title="Lösung" open="false" class="icon"}
H₂ + Cl₂ → 2 HCl
{/sliders}
4. Übung: Ein Kohlenstoffatom soll mit Wasserstoff reagieren. Formuliere hierfür die Reaktionsgleichung in (a) Lewis-Schreibweise und (b) mit Hilfe von Summenformeln.
{slider title="Lösung" open="false" class="icon"}
C + 2 H₂ → CH₄
{/sliders}
-
4.4 Der räumliche Bau von Molekülen
4.4 Der räumliche Bau von Molekülen
{slider title="Link zur interaktiven Übungsseiten mit Bildern" open="false" class="icon"}
Etwas genauer, mit mehr Abbildungen gibt es auf der Basischemie-Seite. Zum Lernen vielleicht besser geeignet. Den Tafelanschrieb gibt es aber komprimierter auf dieser Seite.
Übungsseiten zum räumlichen Bau von Molekülen
{/sliders}
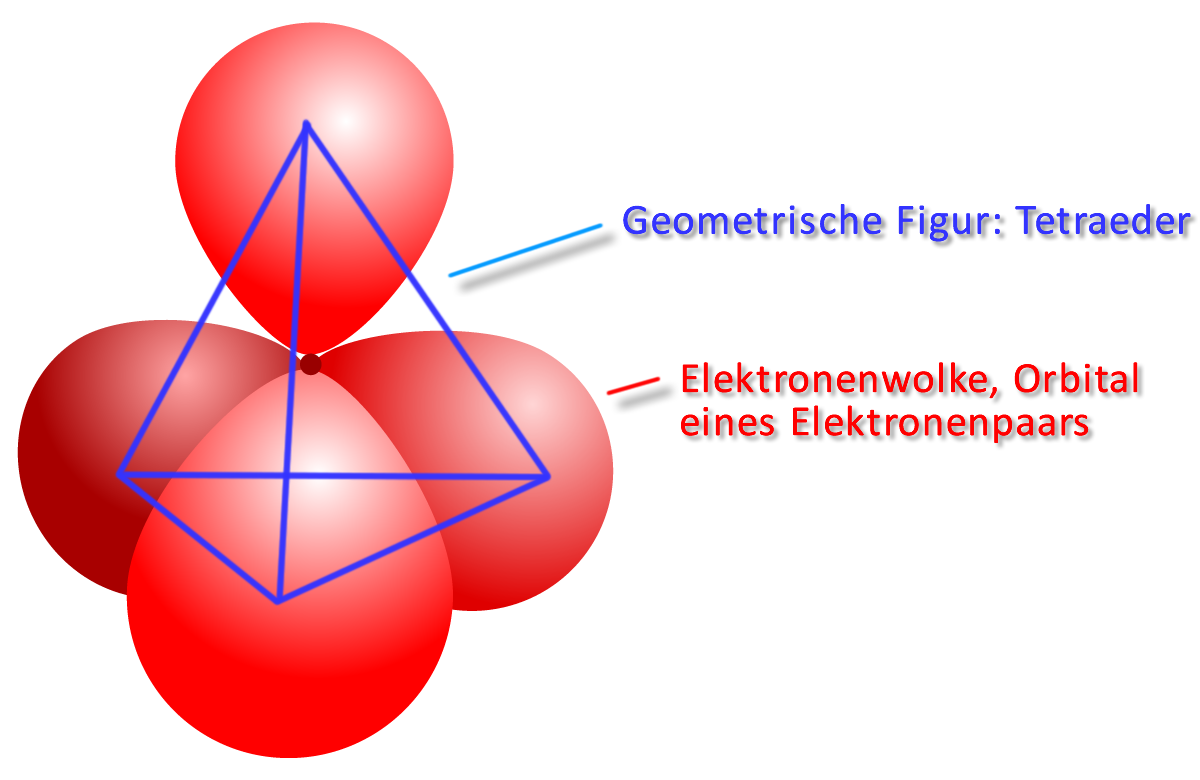
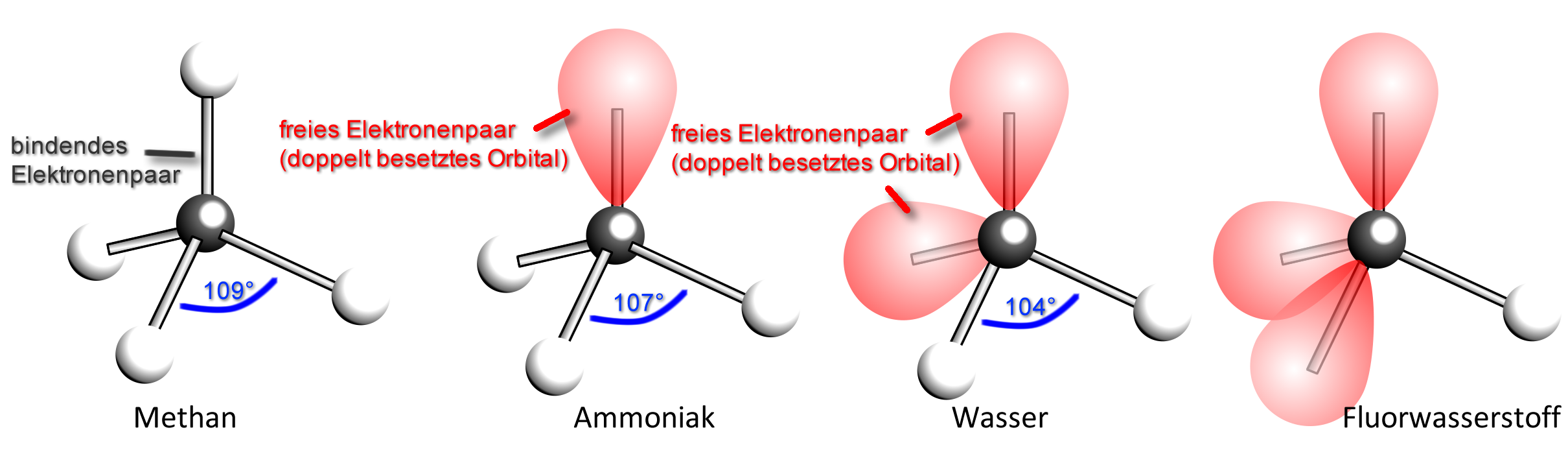
Im Kugelwolkenmodell ordnen sich die vier energetisch gleichwertigen Orbitale tetraedrisch an. Durch die gegenseitige Abstoßung (durch die gleiche, negative Ladung der Elektronen) der „Elektronenwolke“ erreichen sie so den größtmöglichen Abstand voneinander: Tetraederwinkel: 109,5 °
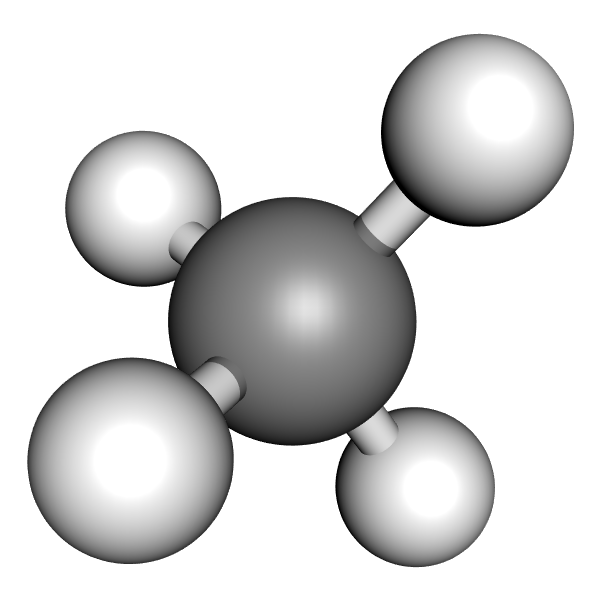
a) Das Methan-Molekül (CH₄)
Die 4 Wasserstoff-Atome sind tetraedrisch um das Kohlenstoff-Atom angeordnet. Die bindenden Elektronenpaare haben somit den größtmöglichen Abstand voneinander.
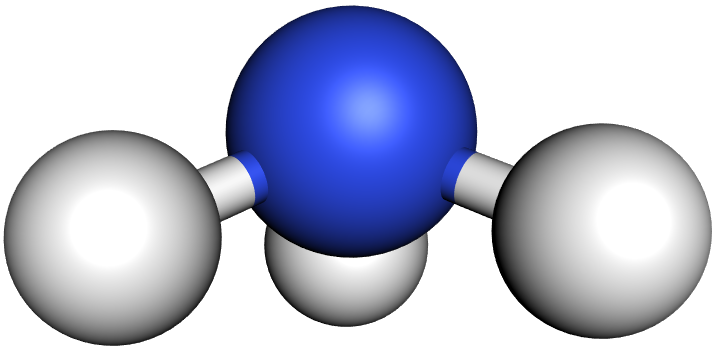
b) Das Ammoniak-Molekül (NH₃):
Im Ammoniak-Molekül stoßen sich die drei bindenden und das eine freie Elektronenpaar gegenseitig ab. Die Winkel zwischen den bindenden Elektronenpaaren sind jedoch nur 107° (statt 109,5°).
Erklärung(durch Zusatzannahmen): Die „Elektronenwolke“ eines nichtbindenden Elektronenpaares nimmt einen größeren Raumbereich ein als die eines Bindungselektronenpaars. Sie drückt daher die anderen „Elektronenwolken“ etwas näher zusammen. Der Bindungswinkel wird kleiner.
Merke: Nichtbindende Elektronenpaare nehmen einen größeren Raum ein als bindende Elektronenpaare. Info für Interessierte: Das oben genanntes Modell ist ein vereinfachtes VSEPR-Modell (Abkürzung für englisch valence shell electron pair repulsion, deutsch Valenzschalen-Elektronenpaar-Abstoßung), auch EPA-Modell (Elektronenpaarabstoßungs-Modell)