Ampholyte
-
4 Allgemeine Säure-Base-Definition nach Brønsted (1923)
4 Allgemeine Säure-Base-Definition nach Brønsted (1923)
a) Säuren...
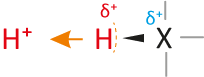
... sind Teilchen, die Protonen abgeben können (= Protonendonator, „Protonenspender“).
Die Teilchen enthalten positivierte H-Atome (Die Bindung zum H-Atom muss polar sein):Wasserstoffatome bestehen nur aus Protonen und Elektronen. Eine Säure besitzt ein Wasserstoffatom, wobei das Elektron von dem Wasserstoffatom „stark“ angezogen wird. Kommt es zu einer Säure-Base-Reaktion (Protolyse), dann wird vereinfacht ausgedrückt nur das Proton des Wasserstoffatoms abgegeben. Das Elektron der Wasserstoffatoms bleibt beim Teilchen zurück (vgl. dazu alle vorher genannten Beispiele).
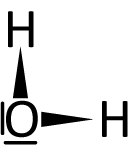
b) Basen...sind Teilchen, die Protonen aufnehmen können (= Protonenakzeptor, „Protonenräuber“). Die Teilchen enthalten mindestens ein freies Elektronenpaar.
Dieses freie Elektronenpaar „nimmt“ dann den positiven Wasserstoffkern (Proton) „auf“.
c) Übung
Im folgenden ist die Lewis-Formel (Strukturformel) von Wasser abgebildet. Gehört dieses Molekül zu einer Brønsted-Säure oder -Base? Schaut Euch dafür nochmals die Definitionen an.
{slider title="Lösung: Was ist Wasser? Eine Säure oder Base?" open="false" class="icon"}
Wasser kann (je nach Reaktionspartner) beides sein. Es kann ein Proton (H⁺) abgeben [es hat ja positivierte Wasserstoff-Atome], wie auch aufnehmen [es hat ja auch freie Elektronenpaare].
Dafür gibt es eine neue Bezeichnung: Wasser ist ein Ampholyt.
{/sliders}
c) Ampholyte
Ampholyte können sowohl als Säuren, wie auch als Basen reagieren. Sie müssen also freie Elektronenpaare (für die Funktion als Basen) wie auch positivierte Wasserstoff-Atome (Funktion als Säure) besitzen.
-
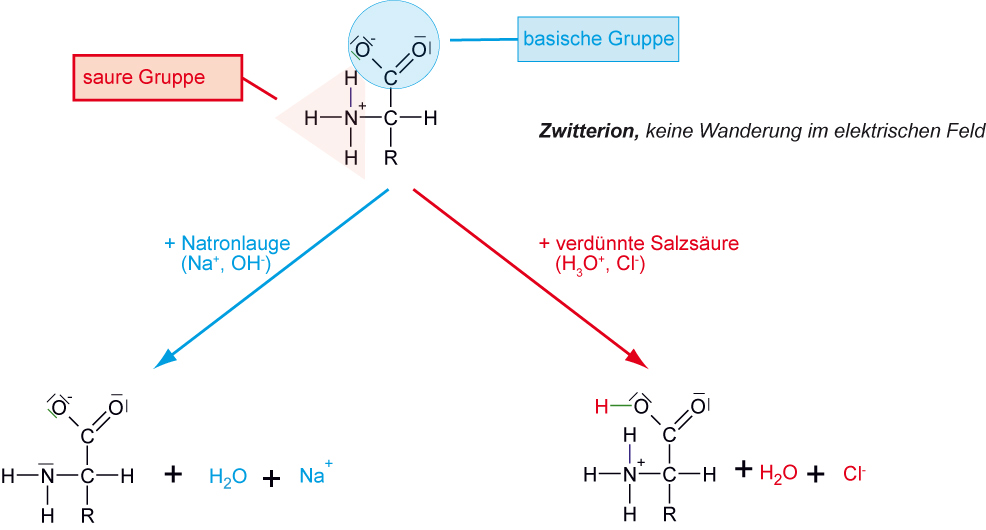
5.1.6 Aminosäure sind Ampholyte
5.1.6 Aminosäure sind Ampholyte
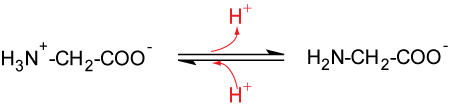
Aminosäuren können sowohl als Brønsted-Säuren als auch als Brønsted-Basen reagieren.
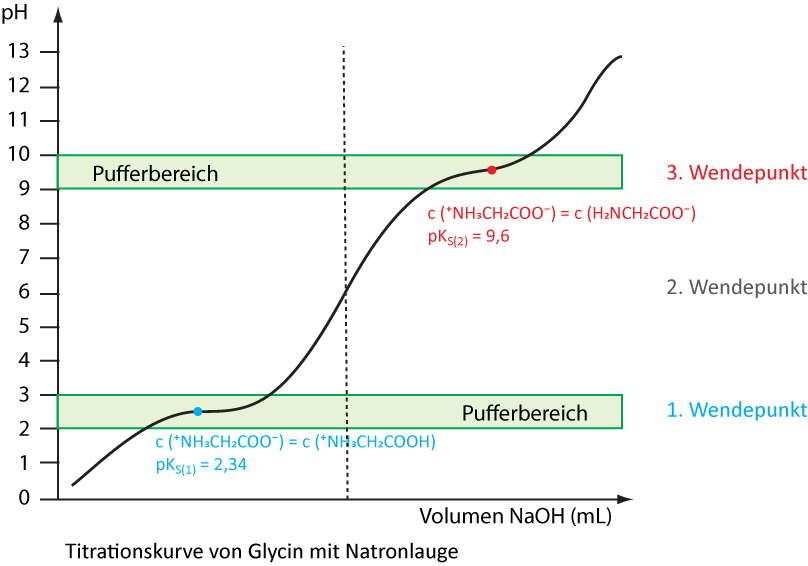
Die hinzugefügten Oxonium- und Hydroxid-Ionen werden abgefangen. Der pH-Wert verändert sich kaum. Aminosäuren besitzen Pufferwirkung.1. Wendepunkt

50 % 50 %
pKS1 = 2,34Für jede Aminosäure gibt es einen pH-Wert, bei dem sie im elektrischen Feld nicht wandert. Diesen pH-Wert bezeichnet man als isoelektrischen Punkt. Bei diesem Punkt liegen praktisch nur die Zwitterionen vor. Der isoelektrische Punkt bei Glycin liegt bei pH 6,0 (2. Wendepunkt).
3. Wendepunkt
50 % 50 %
pKS2 = 9,77 -
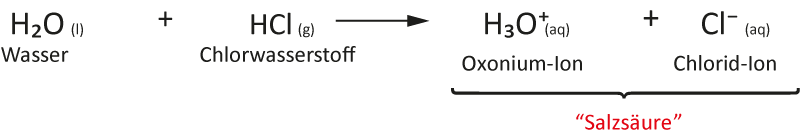
6 Chlorwasserstoff-Gas und Wasser
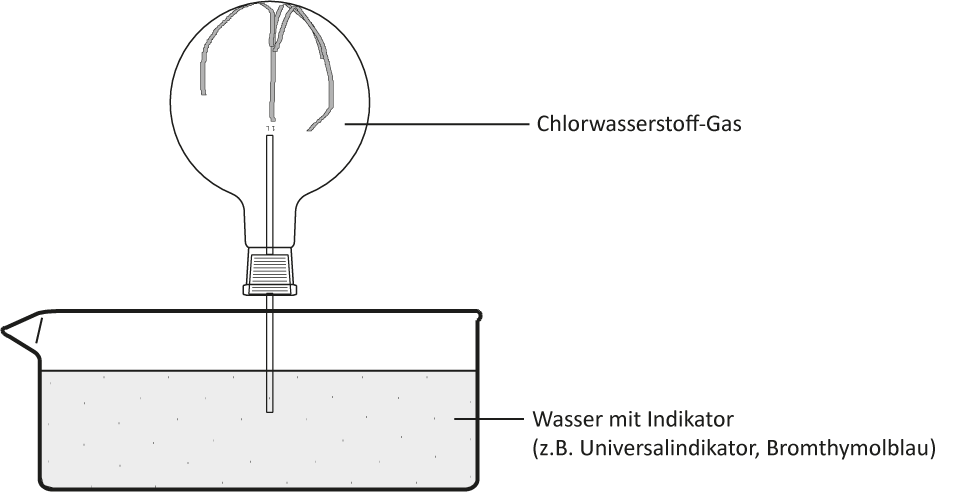
6 Chlorwasserstoff-Gas und Wasser (Springbrunnen)
Chlorwasserstoff: Summenformel HCl, polare Atombindung, Gas, stechender Geruch
Wasser: Summenformel H₂O, polare Atombindung, Flüssigkeit, geruchslos
a) Versuch:
b) Beobachtung:
Das Wasser „schießt“ bergauf in den Rundkolben. Die Indikatorfarbe schlägt nach rot/gelb um. Die rote wässrige Lösung ist geruchlos.c) Reaktionsgleichung – Struktur/Lewisformel:
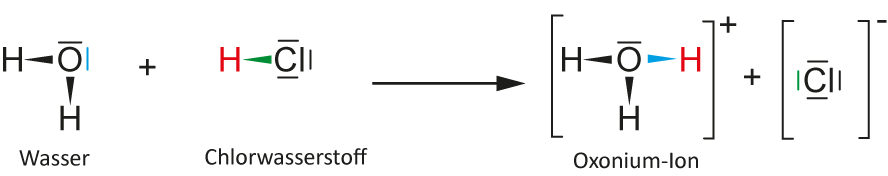
Theoretisch gibt es zwei Möglichkeiten, wie Wasser und Chlorwasserstoff reagieren können.
- Formuliere einmal diese zwei Möglichkeiten als Reaktionsgleichung mit Strukturformeln.
- Entscheide, welche dieser beiden möglichen Reaktionen tatsächlich abläuft. Falls du nicht drauf kommst, gehe zurück zum Thema: Säure-Stärke
{slider title="Lösung" open="false" class="icon"}
1. Möglichkeit:
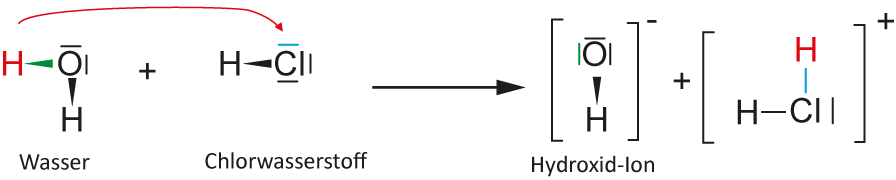
2. Möglichkeit:
Chlorwasserstoff ist die stärkere Säure, da Chlor ein größeres Atom ist, als Wasserstoff. Außerdem ist das Hydroxid-Ion ist eine sehr starke Base.
{/sliders}
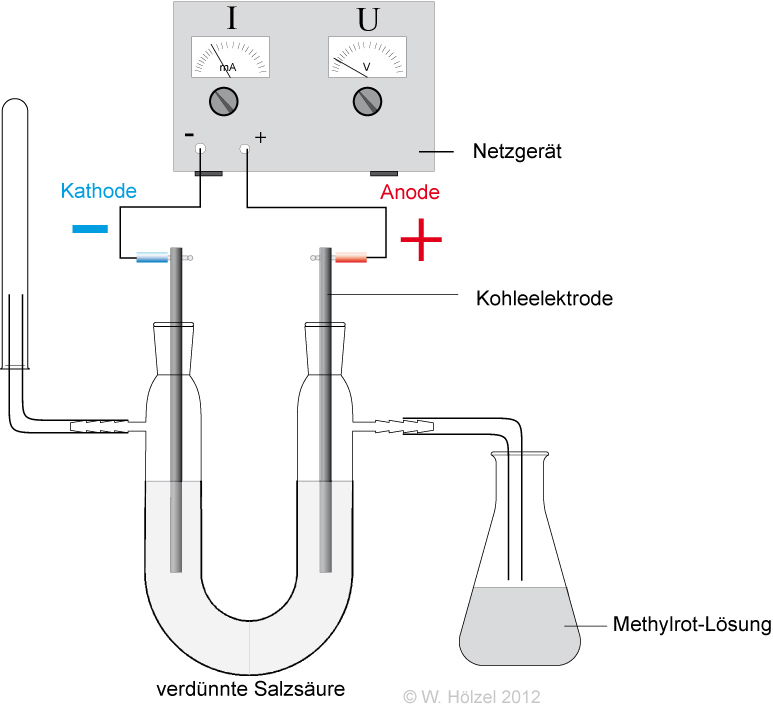
Nachweis der gebildeten Ionen:
- Leitfähigkeitsmessung
- durch Elektrolyse: An der Anode (+-Pol) entsteht dabei Cl₂-Gas. Somit müssen in der verdünnten Salzsäure Chlorid-Ionen (Cl⁻-Ionen) vorliegen.
- durch Indikator: Die Gelbfärbung bei Bromthymolblau zeigt Oxonium-Ionen (H₃O⁺) an.
Reaktionsgleichung Zusammenfassung
{slider title="Lösung" open="false" class="icon"}
Begründung:
Chlor (vom Chlorwasserstoff) ist ein größeres Atom als Sauerstoff (vom Wasser). Deshalb ist Chlorwasserstoff eine stärkere Säure und gibt das Proton (H⁺) und Wasser nimmt das Proton auf.
verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen und Wassermoleküle.{/sliders}
Verdünnte Salzsäure enthält hydratisierte Oxonium- und Chlorid-Ionen und Wassermoleküle.
d) ProtolyseschemaFormuliere für diese Reaktion einmal das Protolyseschema:
{slider title="Lösung" open="false" class="icon"}
{/sliders}
e) Erklärung:
Chlorwasserstoff-Gas reagiert mit Wasser. Im Zylinder entsteht ein Unterdruck. Die Oxonium-Ionen färben den Universalindikator/Bromthymolblau rot/gelb.Salzsäure: = wässrige Lösung des Gases Chlorwasserstoff Wenn man sehr viel HCl-Gas in Wasser einleitet, reagieren nicht mehr alle HCl-Moleküle mit den H₂O-Molekülen. Diese HCl-Moleküle liegen „gelöst“ vor. Es ist so „rauchende“ bzw. konzentrierte Salzsäure entstanden.
Leitfähigkeit Geruch Indikatorpapier Teilchen verdünnte Salzsäure + - rot H₂O, H₃O⁺, Cl⁻ rauchende Salzsäure + + rot H₂O, H₃O⁺, Cl⁻, HCl